Образование - комплекс - железо
Cтраница 2
 |
Концентрация различных солей в моноэтаноламина С при 25 С, % ( масс. [16] |
В процессе регенерации при повышенной температуре возможно образование комплексов железа с. [17]
 |
Концентрация различных солей в моноэтаноламина С при 25 С, % ( масс. [18] |
В процессе регенерации при повышенной температуре возможно образование комплексов железа с МЭА хелатного типа в виде триэтаноламинового железа. При охлаждении и взаимодействии этих соединений с H2S выпадает осадок сернистого железа. [19]
Превосходный, чувствительный метод определения железа основан на образовании оранжево-красного комплекса железа ( II) с 1 10-фенантролином, формула которого дана в гл. [20]
По-видимому, как только система становится сопряженной, основным условием образования стабильного трикарбонильного комплекса железа является наименьшая пространственная компактность. [21]
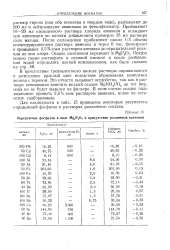 |
Определение фосфатов в виде Mg2P2O7 в присутствии различных катионов. [22] |
В присутствии трехвалентного железа растворы окрашиваются в интенсивно красный цвет вследствие образования комплекса железа с тироном. Это отчасти вызывает неудобство, так как в растворе невозможно заметить мелкий осадок MgNH4PO4 до тех пор, пока он не будет выделен на фильтре. В этом случае осадок надо тщательно промыть 2 5 % - ным раствором аммиака, иначе он оста-нется слаборозовым. [23]
Установлено, что в ходе каталитического окисления в фазе полимера происходит образование сульфидных комплексов железа. В повторных опытах каталитическая активность гидрогелей изменяется и зависит от состава комплексов в фазе гидрогеля. В некоторых случаях наблюдаются эффекты разработки полимерных катализаторов - которые, по-видимому, связаны с наличием подвижной полимерной матрицы и изменением состава комплексов железа ( Ш) и железаШ) в ходе катализа. [24]
Пока не достигнута точка эквивалентности, концентрация остающихся в растворе ЗСЫтюнов настолько мала, что образования комплексов железа, в частности P7e ( SCN) 2, не происходит. Но первая же избыточная капля раствора NH4SCN повысит эту концентрацию настолько, что указанная реакция произойдет и раствор приобретет более или менее интенсивную оранжево-красную окраску. [25]
Несколько другой путь расчета констант устойчивости был избран Матту [7], который также определил константы образования комплексов железа ( III) с сульфосалициловой кислотой из экспериментальных данных Варейля. [26]
Данные табл. 3.9 показывают, что определение целого ряда функций основывается прямо или косвенно на образовании гидр-оксамовых комплексов железа. В число определяемых соединений входят сложные эфиры, карбоновые кислоты, галогенангидриды и ангидриды кислот, спирты и изоцианаты. Некоторые из характерных для этих соединений групп можно отличать друг от друга, используя соответствующие модификации метода. [27]
Наиболее распространенным принципом, лежащим в основе определения органических кислот и ряда их производных, является образование гидроксамовых комплексов железа. [28]
В качестве измеряемого свойства было использовано ослабление окраски раствора, связанное с разрушением окрашенного роданидного и образованием бесцветного фторид-ного комплекса железа. Сливаемые растворы, содержащие в 1 л по 0 4 10 - 3 моль соответственно окисного железа и фторида натрия. [29]
Данные табл. 10 отражают влияние на Е как ионной силы раствора, так и влияние конкурирующей реакции образования комплексов железа ( 111) с соответствующим анионом. [30]
Страницы: 1 2 3 4