Образование - лактон
Cтраница 1
Образование лактонов непосредственно из соответствующих окси-кислот вполне аналогично этерификации карбоповых кислот; разница заключается только в том, что в первом случае реагирующие друг с другом карбоксил и гидроксил принадлежат одной молекуле, а при обь № ной этерификации - двум различным молекулам. [1]
Образование лактона ( 51) показывает, что кладиноза представляет собой альдозу. По спектральным данным последняя имеет полуацеталь-ное строение. В отличие от кладинозы ее метилгликозид не дает иодо-формной реакции, откуда следует, что в образовании окисного кольца участвует О-атом при Cs и, следовательно, кладиноза должна являться пиранозой. [2]
Образование лактонов с более удаленной группой ОН ( больше 7 атомов С в молекуле) затруднено; их получают нагреванием ю - О. [3]
Образование лактона V доказывает, что спиртовые группы несут цепи, занимающие соседние позиции. То же доказывает замыкание двухосновной кислоты VI, получившейся после окисления лактона, в циклический ангидрид VII. Наконец, при энергичном окислении в щелочной среде исчезает метил и образуется трехосновная кислота VIII, при нагревании декарбоксилирующаяся в двухосновную кислоту, способную давать ангидрид IX. Кислота VIII дает характерную для а-пиридинкар-боновых кислот окраску с хлорным железом, которую двухосновная кислота, соответствующая ангидриду IX, не дает. Фенольная оксигруппа пиридоксола занимает другое р-положение, что было установлено на основании аналогии УФ-спектров пиридоксола и р-оксипиридина. [4]
Образование лактона V доказывает, что спиртовые группы несут цепи, занимающие соседние позиции. То же доказывает замыкание двухосновной кислоты VI, получившейся после окисления лактона в циклический ангидрид VII. Наконец, при энергичном окислении в щелочной среде исчезает метил и образуется трехосновная кислота VIII, при нагревании декарбоксилирующаяся в двухосновную кислоту, способную давать ангидрид IX. Кислота VIII дает характерную для а-пиридинкарбоновых кислот окраску с хлорным железом, которую двухосновная кислота, соответствующая ангидриду IX, не дает. Фенольная оксигруппа пиридоксола занимает другое - положение, что было установлено на основании аналогии УФ-спектров пиридоксола и 3-оксипиридина. [5]
Никаких признаков образования лактона из этиленгликоля и янтарной кислоты в нормальных условиях не наблюдается, хотя лактон и может быть получен. Со щавелевой кислотой образование лактона проходит гладко, невидимому, потому, что он состоит скорее из шести, чем из восьмичлепнот кольца. [6]
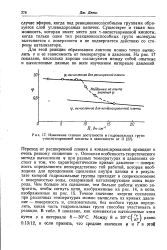 |
Изменение степени доступности р гидроксильных групп f - оксистеариновой кислоты в зависимости от П. [7] |
Для этой реакции образования лактона можно точно вычислить 9 и ее зависимость от температуры и давления. [8]
Особенно интересный пример образования лактонов был изучен Бартоном в связи с выяснением стереохимии тритерпенов группы р-амирина. Как хорошо известно, обработка у-ненасыщен-ных кислот сильными кислотами обычно приводит к лактонам. Бартон и Холнесс [128] использовали это свойство в своей изящной работе по изучению стереохимии сочленения колец C / D в олеаноловой кислоте GGXLVI. При пропускании хлористого водорода в раствор этой кислоты в хлороформе образуется равновесная смесь, содержащая 24 % лактона CCXLVII. Поскольку лактон GCXLVII не способен превращаться в CCXLVIII, а дает лишь CGXLVI, следовательно, водород при С-18 находится в tywc - положении по отношению к кислороду при С-13. Этот вывод согласуется с известным положением о затрудненности ионного tyuc - отщепления ( см. стр. С-12, приводящее к исходному веществу CGXLVI. Следовательно, кольца D и Е должны иметь мс-сочленение, а карбоксильная группа должна быть аксиальной. [9]
Изучая внутримолекулярную реакцию образования лактонов, в которой наблюдается увеличение скорости на 3 - 6 порядков по сравнению с бимолекулярной реакцией, Кошланд [65] предложил новое понятие - орбитальное управление. Исходя из экспериментов, он предположил, что управление атомами может вызвать ( или объяснить) высокие скорости реакции. Реагирующие группы не только должны быть сближены, но и правильным образом ориентированы. При использовании таких представлений важную роль играют эффекты и сближения, и ориентации. В более жестких молекулах реакция идет с большей скоростью. [10]
Образование лактамов аналогично образованию лактонов из кислот ( стр. [11]
Образование лактамов аналогично образованию лактонов из у-окси-кислот ( стр. [12]
Образование лактамов аналогично образованию лактонов из оксикислот ( см. стр. [13]
Его строение доказывается образованием лактона, озонирование которого дает соответствующий кетолактон и формальдегид. [14]
Потенциал, необходимый для образования лактона ( см. уравнение 14.8), такой же, что и потенциал, необходимый дтя окисления родственного циклоач-кена. В сопоставимых условиях насыщенные карбоксилаты не подвергаются значительному окислению при потенциале меньше 2 4В ( отн. Ag), как было показано с помощью циклической вольтампсрометрии. [15]
Страницы: 1 2 3 4