Образование - ионные пары
Cтраница 2
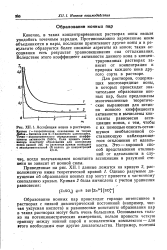 |
Ассоциация ионов в растворах. [16] |
Образование ионных пар происходит гораздо интенсивнее в растворах с низкой диэлектрической постоянной ( например, чистая уксусная кислота) и равновесные константы образования пар в таких растворах могут быть очень большими. Основываясь только на потенциометрических измерениях, нельзя провести четкую границу между ионной парой и ковалентным комплексом - для этого необходимы еще другие доказательства. [17]
Образование ионных пар благоприятствует димеризации анион-радикалов, поскольку ионы металла стабилизуют отрицательно заряженные центры ди-аниона типа ( 32) и уменьшают кулоновское отталкивание между ними. С другой стороны, использование растворителей с высокой диэлектрической проницаемостью приводит к разделению ионных пар и равновесие смещается в сторону анион-радикала. [18]
 |
К расчету энергии иона в мембране. а - влияние сил изображения, б - образование ионных пар, в - гидрофильная пора в мембране, г - влияние комплексообразоваяия. [19] |
Образование ионных пар также не дает заметного выигрыша - максимальное понижение энергии не более чем двукратное. [20]
Образование ионных пар и их адсорбция на электроде являются, по Гирсту, причиной появления анионного специфического эффекта. [21]
Образование ионных пар возможно в том случае, если электростатическое взаимодействие между ионами больше, чем их средняя кинетическая энергия. Незаряженные ионные двойники отличаются от обычных диссоциированных молекул электролита лишь природой сил взаимодействия, хотя не исключена возможность того, что ионы в двойнике отделены друг от друга молекулами растворителя. Обычно принимается, что распад и образование ионных пар не требует в отличие от обычных молекул никакой энергии активации. Такое заключение вряд ли можно принять безоговорочно, так как эти процессы сопровождаются изменениями сольватных оболочек, что связано со значительными энергетическими эффектами. [22]
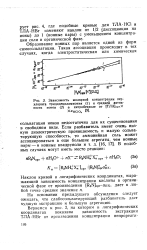 |
Зависимость молярной концентрации перхлората тридодециламмония ( 1 и средней активности ионов ( 2 в нитробензоле от [ ГЛА ] 0ргХ. [23] |
Образование ионных пар является одной из форм самосольватации. [24]
Образование ионных пар можно рассматривать по Кольтгофу как процесс ионизации, а распад ионных пар на ионы - как процесс диссоциации. [25]
Образование ионных пар в этой реакции рассматривается в обзорах: Bartsch, Zdvada, [4]; Bartsch, Асе. [26]
Образование ионных пар можно рассматривать по Кольтгофу как процесс ионизации, а распад ионных пар на ионы - как процесс диссоциации. [27]
Образование ионных пар наряду с кинетическими эффектами существенно влияет на эффективную устойчивость комплексных ионов. [28]
Образованием ионных пар объясняется также большая способность катионообменников различного типа ( в том числе гелей цеолита и сульфокислотных смол) к поглощению катионов тяжелых металлов ( Ag, Tl, РЬ2 и др.) и избирательная сорбция калия дипикриламиновой смолой, полученной Скогсайдом. [29]
Идентифицировать образование ионных пар в растворах несимметричных электролитов еще труднее, чем в симметричных электролитах, так как ионные пары несимметричных электр олитов обладают свободным зарядом ( например, NaSCU, ВаС1), и поэтому они принимают участие в переносе электричества. [30]
Страницы: 1 2 3 4