Образование - центр - кристаллизация
Cтраница 2
Если образование центров кристаллизации и рост кристаллитов нельзя изучать раздельно, то можно проследить за интегральным эффектом превращения аморфного материала в кристаллический с помощью какого-либо метода, позволяющего определить степень кристалличности. Например, можно проводить измерения удельного объема, поместив кристаллизующийся образец в дилатометр. [16]
Если образование центров кристаллизации при зарождении новой фазы вещества внутри другой его фазы, например при конденсации в водяных парах капель жидкости или при возникновении кристаллов в расплаве, происходит в отсутствии или без помощи посторонних частиц, то такой процесс Стуки [119] определяет как гомогенную кристаллизацию в отличие от гетерогенной, или катализированной кристаллизации, когда центры кристаллизации новой фазы образуются на поверхностях, имеющих отличный от этой новой фазы химический состав. [17]
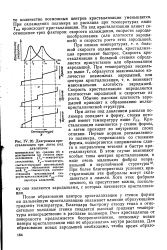 |
Диаграммы кристаллизации при литье под давлением. [18] |
После образования центров кристаллизации у стенок формы на дальнейшую кристаллизацию оказывает влияние образующийся градиент температуры. Благодаря быстрому отводу тепла в относительно холодные стенки создается высокий градиент температуры непосредственно в расплаве полимера. Рост кристаллитов от поверхности продолжается беспрепятственно, поскольку новые центры кристаллизации еще не образовались внутри расплава. [19]
После образования центров кристаллизации при продолжающейся эмульсификации идет их рост за счет вновь образующегося галогенида серебра; при этом происходит и частичное слипание центров. В процессе роста центров ионы кристаллизующегося вещества должны преодолеть сопротивление адсорбционного слоя ионов или молекул на поверхности кристалла. Таким образом, процесс кристаллизации состоит из двух фаз: диффузии кристаллизующегося вещества через слой, адсорбированный на поверхности кристалла, и перехода ионов этого вещество из полуориентированного состояния в упорядоченное состояние кристаллической решетки. Если скорости этих фаз сильно различаются, общую скорость процесса определяет скорость более медленной фазы, в случае получения фотографической эмульсии - скорость диффузии ионов. [20]
После образования стабильных центров кристаллизации они продолжают расти со скоростью, определяемой условиями и степенью переохлаждения. Это деление кристаллизации на стадии условно, и практически обе стадии накладываются друг на друга. [21]
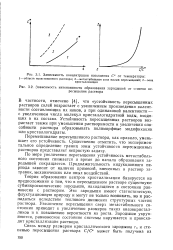 |
Зависимость концентрации насыщения С от температуры.| Зависимость интенсивности образования зародышей от степени пересыщения раствора. [22] |
Теория образования центров кристаллизации базируется на предположении о том, что в пересыщенном растворе существуют субмикроскопические зародыши, находящиеся в состоянии равновесия с раствором. Эти зародыши имеют статистическую, флуктуационную природу и могут не только возникать, но и распадаться вследствие теплового движения структурных частиц раствора. Увеличение пересыщения сверх метастабильного состояния приводит к увеличению размеров таких квазикристалликов и к повышению вероятности их роста. Зародыши укрупняются, равновесное состояние системы нарушается и происходит кристаллизация раствора. [23]
 |
Зависимость концентрации насыщения ( растворимости от температуры. [24] |
Теория образования центров кристаллизации базируется на гипотезе о том, что в пересыщенном растворе изначально существуют некие субмикроскопические зародыши, находящиеся в термодинамическом равновесии с раствором. Эти зародыши имеют статистическую, флуктуационную природу и могут не только самопроизвольно возникать в местах случайного скопления молекул растворенного вещества, но и распадаться вследствие теплового движения структурных частиц ( молекул) раствора. Увеличение степени пересыщения раствора сверх метастабильного состояния ведет к возрастанию размеров таких квазикристалликов и к увеличению вероятности роста их размеров. Зародыши укрупняются, равновесие между ними и пересыщенным раствором нарушается, вследствие чего происходит кристаллизация растворенного вещества. По мере кристаллизации избыток растворенного вещества сверх его количества, соответствующего насыщенному состоянию раствора, выделяется в виде кристаллов. [25]
Вероятность образования центров кристаллизации резко падает при уменьшении пересыщения. [26]
Скоростью образования центров кристаллизации называется число центров кристаллизации, ежесекундно возникающих в единичном объеме расплава. [27]
Скорость образования центров кристаллизации становится зависимой от скорости диффузии атомов или молекул через границу раздела фаз в случае, если одна или обе фазы представляют собой вязкую жидкость или твердое тело. [28]
Процесс образования центров кристаллизации обратим. Даже при сравнительно высоких температурах при беспрерывном движении молекул в жидкости возможны случаи образования центров кристаллизации. Но из-за быстрого поступательного движения частицы, образующие такой кристалл, удаляются друг от друга, и центр кристаллизации распадается. Таким образом, происходит все время обратимый процесс образования и распада центров кристаллизации. С понижением температуры и связанным с этим уменьшением скорости движения молекул и ионов некоторые из образовавшихся центров кристаллизации не распадаются, а сохраняют упорядоченное расположение молекул. В общем движении молекул жидкости такие центры кристаллизации при соответствующих температурных условиях представляют собой отдельные агрегаты, передвигающиеся в жидкости одновременно с ее молекулами и ионами. [29]
Скорость образования центров кристаллизации не будет расти бесконечно по мере снижения температуры, так как второй экспоненциальный член начинает играть определяющую роль. [30]
Страницы: 1 2 3 4 5