Образование - пятичленный цикл
Cтраница 3
О в транс - 1 2-дио-ле ( 2) ( использовался как один из стандартных образцов) равно 2 34 А. O uc - изомера может быть объяснено легкостью образования пятичленного цикла с водородной связью. Таким образом, движение в направлении, показанном стрелкой в структуре ( I), в конечном счете приведет к инвертированной форме кресла и требует меньшей энергии, в то время как движение в структуре ( II) приводит к большему сплющиванию кресла. Такая легкость в образовании пятичленного кольца из са связей ( связи цис-1 2) по сравнению с ее связями ( связи транс-1 2) отражается и в большей чувствительности цис-ддолов к окислению и образованию комплексов с борной кислотой. Это происходит потому, что для этиленгликоля невозможна заслоненная конформация с взаимодействием несвязанных атомов. [31]
Дело в том, что в данном случае напряжение в циклах, возникающее при деформации валентных углов в лиганде, минимально. Для комплексообразовате-лей с координационным числом 2 и линейной структурой образование пятичленного цикла может привести к такой сильной деформации лиганда, что подобный хелатный комплекс может вробще не образоваться. [32]
Очевидно, что сближенные атомы ( если они содержат при себе какие-то активные группы) могут взаимодействовать друг с другом химически. В этом геометрическая причина давно известной из опыта сравнительной легкости образования пятичленных циклов. [33]
Донорные лиганды показывают возрастающую тенденцию к образованию трех - и четырехчленных циклов. Такие циклы образуются в тех случаях, когда нет возможности к образованию пятичленного цикла. [34]
Присоединение диазосоединения к олефину или ацетилену рассматривается как 1 3-биполярное циклоприсоединение. Этот диполь присое диняется к ненасыщенному партнеру ( диполярофилу) с циклическим сдвигом электронов и образованием пятичленного цикла. [35]
Так, 1-хлорантрон - 9 ( 56) получают из 1-хлорантрахинона действием порошка алюминия в 95 % - ной H2SO4 в присутствии NaaSCU при 35 - 40 С. Дальнейшие стадии синтеза аналогичны описанным выше, но вследствие ориентирующего влияния атомов хлора в а-положениях в образование пятичленных циклов вовлекаются атомы углерода, находящиеся в пара-положении к атомам хлора. [36]
Таким образом, в изученных условиях ( Pt / C, 310 С) З - этилпентен-2 не только не ускорял реакцию циклизации 3-этилпептана, но отчетливо тормозил ее. Следовательно, можно думать, что в присутствии Pt / C в названных условиях главный путь образования пятичленного цикла исключает промежуточную стадию дегидрирования парафинов в олефины. Этот факт, примечательный сам по себе, представляется особенно интересным, поскольку известно, что реакция Св-дегидроциклизации алканов в присутствии окисных [2] и ряда металлических [3, 4] катализаторов проходит по консе-кутивной схеме: парафин - олефины - - ароматические углеводороды. [37]
Каталитическая роль полухлористой меди сводится к. Предполагается, что вначале образуется комп лекс, приводящий к неполярному переходному состоянию [23], в котором равновероятна атака по любому углеродному атому тройной связи. При этом легкость образования пятичленных циклов по сравнению с шестич-ленными является определяющим фактором. [38]
Поэтому процесс циклизации более вероятен, чем образование амида. Внутримолекулярная циклизация с образованием пяти-членного цикла, которая, например, происходит при атаке у атома кислорода в производных мочевины, в случае производных формамида и ацетамида54 невозможна. Для того чтобы произошла циклизация с образованием пятичленного цикла, необходимо наличие двух радикальных центров в одной молекуле или такая атака радикала на нейтральную группу, которая приведет к отщеплению атома фтора или водорода. Оба указанных процесса менее вероятны, чем гликоколь-оксазол-идиновая циклизация, и в этих случаях происходит предпочтительное образование амидов. [39]
Интересно отметить, что некоторые пятичленные циклы легко превращаются в десятичленные. Например, 1 1-дибутокси - 1-сила - 2-оксациклопентан при стоянии при комнатной температуре переходит в 1 1 6 6-тетрабутокси - 1 6-дисила - 5 10-диоксациклодекан. При нагревании может проходить обратная реакция с образованием пятичленного цикла. [40]
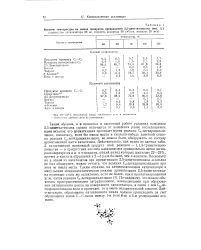 |
Влияние температуры на выход продуктов превращения 2 5-диметилгексана ( вес. %. [41] |
Таким образом, и в принятых в настоящей работе условиях поведение 2 5-диметилгексана сильно отличается от поведения ранее исследованных нами октанов: его ароматизация протекает путем реакции Св-дегидроцикли-зации, поскольку, если бы имела место в сколько-нибудь заметной степени реакция С5 - дегидроциклизации, ее можно было обнаружить по составу ароматической части катализата. Поскольку ни в одном из катализатов при ароматизации 2 5-диметилгексана ж-ксилол не был обнаружен, можно считать, что реакция С5 - дегидроциклизации при этом не имела места. По-видимому, это можно объяснить пространственными затруднениями, возникающими при образовании пятичленного цикла на поверхности катализатора, в связи с чем С5 - де-гидроциклизация если и протекает, то в очень незначительной степени. Действительно, образование пятичленного цикла должно происходить за счет образования новой С-С - связи между 1 - м ( или 8 - м) и 5 - м углеродными атомами. [42]
Реакции диэтилоксалата с тиосемикарбазидом были проведены в присутствии метилата натрия в среде метилового спирта и в среде этанола в присутствии свежепрокаленного ацетата натрия. Наибольший выход триазина ( 2) был получен в метиловом спирте в присутствии метилата натрия ( 19 %), наименьший ( 9 %) - в этиловом спирте в присутствии ацетата натрия. Низкий выход целевого триазина, возможно, связан с тем, что для тиосемикарбазида характерно таутомерное равновесие: гидразид тиокислоты меркаптогидразон, и это равновесие больше смещено в сторону меркаптогидразона, предположительно, вступающего в реакцию с диэтиловым эфиром щавелевой кислоты с образованием пятичленного цикла, который выделить не удалось. [43]
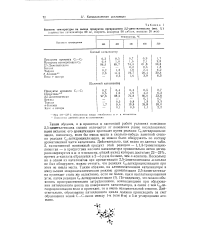 |
Влияние температуры на выход продуктов превращения 2 5-диметилгексана ( вес. %. [44] |
Таким образом, и в принятых в настоящей работе условиях поведение 2 5-диметилгексана сильно отличается от поведения ранее исследованных нами октанов: его ароматизация протекает путем реакции Св-дегидроцикли-зации, поскольку, если бы имела место в сколько-нибудь заметной степени реакция С5 - дегидроциклизации, ее можно было обнаружить по составу ароматической части катализата. Поскольку ни в одном из катализатов при ароматизации 2 5-диметилгексана ж-ксилол не был обнаружен, можно считать, что реакция С5 - дегидроциклизации при этом не имела места. По-видимому, это можно объяснить пространственными затруднениями, возникающими при образовании пятичленного цикла на поверхности катализатора, в связи с чем С5 - де-гидроциклизация если и протекает, то в очень незначительной степени. Действительно, образование пятичленного цикла должно происходить за счет образования новой С-С - связи между 1 - м ( или 8 - м) и 5 - м углеродными атомами. [45]
Страницы: 1 2 3 4