Образование - циклопропан
Cтраница 3
В этой связи большой интерес представляет гидролиз у-галогенпропил-боранов, получаемых при добавлении диборана к соответствующему аллил-галогениду, также приводящий к образованию циклопропанов. [31]
Через согласованное 1 3-диполярное присоединение диазосоединения к кратной связи олефина, образование 1-пиразолина и распад последнего с выделением азота и образованием циклопропана. [32]
Первая стадия - это медленное превращение пиразолина-2 в пиразолин-1 [15], а вторая, быстрая стадия представляет собой стереоспецифическое отщепление N2 с образованием циклопропана. [33]
Поэтому предположение, что продукт 62 - D3 образуется из 1-пропильного катиона после 1 3-гид-ридного сдвига, сомнительно, и, следовательно, увеличивается вероятность образования циклопропана путем депротонирования промежуточно образующегося протонированного по ребру циклопропана, как описано в предыдущем разделе. [34]
Восстановление а р-ненасыщенных кетонов в алкены обычно проводят десулъфированием дитиокеталей с использованием скелетного никеля [ реакция (8.12) ], поскольку метод Кижне-ра - Вольфа приводит к образованию циклопропана [ реакция (8.13) ] через пиразолин ( 29), а кислотные условия реакции Клемменсена для этих соединений не подходят. [35]
Дихлоркарбен является очень электронодефицитной частицей и ( если генерируется в апротонном растворителе) присоединяется к двойной связи богатых электронами алкенов, например цис-бутену-2 ( 79) с образованием циклопропанов, например ( 80), - реакция улавливания ( ср. [36]
В реагенте 225 эта проблема решается правильным выбором защиты спиртового гидроксила: защищенный гид-роксил образует ацеталь, являющийся плохой уходящей группой в реакциях нуклеофильного замещения, что исключает возможность образования циклопропана. Кроме того, и это немаловажно, удаленно этой защиты требует весьма мягких условий, что устраняет опасность элиминирования на заключительных стадиях. [37]
Конечно, приведенные результаты можно было бы объяснить только на основании известных реакций карбенов - без привлечения илида ХЖ, однако последний был выделен в индивидуальном виде, и его участие в образовании циклопропана хх и не вызывает сомнений. [38]
Существует предположение, что эти продукты образуются в результате следующих реакций: часть диазоуксусного эфира превращается в эфир фумаровой кислоты, который затем конденсируется89 с неизмененным диазоуксусным эфиром, и часть его в дальнейшем пиро-лизуется с образованием производного циклопропана. При нагревании эфира пиразолин-трикарбоновой кислоты можно получить триэтиловый эфкр транс-циклопропан-1 2 3-трикарбоновой кислоты. Метиловый эфир ведет себя аналогично. [39]
По непонятной причине перегруппировки, протекающие по этому механизму, стали называть квази-перегруппировками Фаворского, хотя именно при реализации этого механизма происходит перестройка скелета с 1 2-смещением группы; при течении же по циклопропановому механизму образование молекулы с измененным скелетом происходит вследствие возникновения связи между одними атомами при образовании циклопропана, а при его нарушении разрыва связи между соседними. [40]
Перегруппировка [56] бис ( метоксикарбонил) метилида тиофения в 2-замещенный тиофен послужила прообразом реакции тиофена с этилдиазо-ацетатом [57], в результате которой, как полагают, образуется продукт присое -: карбена по двойной связи 2 3; возможно, процесс идет через первона-атаку по атому серы с последующей перегруппировкой S - С и образование циклопропана. [41]
Полоса поглощения при К С 2600 А; при облучении полным светом в жидкой фазе основными продуктами являются окись углерода, двуокись углерода, циклопропан, этилен, аллилформиат, циклопропане л, пропионовый альдегид и ацетальдегид; из начальных наклонов кривых зависимости выхода продуктов от времени получаются следующие относительные начальные скорости образования: 1 0 ( аллилформиат), 0 7 ( ацетальдегид), 0 0 ( циклопропанол), 0 05 ( пропионовый альдегид), 0 08 ( циклопропан), 0 14 ( этилен), 0 08 ( двуокись углерода); циклопропанол может образоваться при вторичном фотолизе первичных продуктов. Образование циклопропана, ацетальдегида, аллилформиата и этилена тормозится олефинами ( цс-бутеном-2 или г цс-пентеном-2), которые изомеризуются; поэтому для этих продуктов вероятно триплетное исходное состояние. [42]
В определенных условиях ( ТГФ, низкая температура) ответственными за образование циклопропанов при реакциях с олефинами могут быть а-галоидзамещенные ( карбе-ноидные) литийорганические соединения ( см. гл. Образование циклопропанов оказалось реакцией, характерной как для карбенов, так и для карбеноидных литийорганических соединений, стр. [43]
В принципе в приведенных интермедиатах не исключена возможность равновесного перемещения протона, например так, как изображено на схеме ( см. стр. Образование протонирован-ного циклопропана часто постулируется для объяснения экспериментальных фактов. [44]
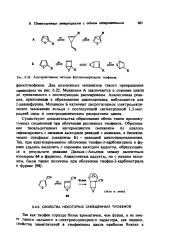 |
Альтернативные методы фотоизомеризации тиофенов. [45] |
Страницы: 1 2 3 4