Поверхностный окисел
Cтраница 3
Для атомов, находящихся внутри базисных плоскостей и обладающих одной остаточной валентностью, поверхностный окисел может быть представлен схемой А. Окисел типа А образуется при малых давлениях кислорода от 10 - 5 до 2 мм рт. ст.; он устойчив при высоких температурах. [31]
Рассмотрим теперь следующие процессы, которые происходят на поверхности: 1) образуется поверхностный окисел типа 1; 2) образуется поверхностный окисел типа 2; 3) поверхностный окисел типа 1 покидает поверхность; 4) поверхностный окисел типа 2 покидает поверхность; 5) свободные места типа 1 превращаются в места типа 2 с константой скорости первого порядка k3; 6) поверхностный окисел типа 1 становится на место окисла типа 2; константа скорости для этого процесса первого порядка k4; 7) места типа 2 превращаются в места типа 1 со скоростью, которая пропорциональна числу мест типа 2 и скорости, с которой окисел типа 1 покидает поверхность. Скорость этого процесса дается выражением ( I / a) k - ( 1 - f) N, где 1 / а - коэффициент пропорциональности. Возможность процесса 7 будет показана, когда будет обсуждаться физическая интерпретация кинетики. [32]
Наличие резервов легко усмотреть из схем разрезов решеток металла и сопрягающегося с ним поверхностного окисла ( рис. 34 - 39), где черными кружками помечены ионы металла в решетке окисла и металлические ядра в металле. Все пространство между этими ядрами может быть занято частицами неметалла при их проникновении в металлическую решетку. Это не значит, что резервные объемы таковы, что при образовании нормального окисла в металлической решетке найдется место для всего количества кислорода, соответствующего стехиометриче-ским отношениям. [33]
Количество электричества, необходимое для пассивации железного электрода, зависит от условий образования поверхностного окисла. [34]
В данном случае электрон, выходящий из металла в раствор, должен пройти через поверхностный окисел и находящийся на нем двойной слой. Поэтому величина 10 у в уравнении ( 3) оказывается одинаковой и для объема, и для поверхностного слоя электрода. [35]
Для наиболее активных атомов углерода, связанных с решеткой одной валентностью, характерным является поверхностный окисел типа С. [36]
Подобным же образом при движении в катодном направлении, за исключением крайних анодных поляризаций, поверхностный окисел полностью восстанавливается, прежде чем произойдет заметная хемосорбция водорода из раствора. [37]
С помощью предлагаемого метода на примере серебра в щелочном растворе установлена связь между отклонением от стехиометрии поверхностного окисла и потенциалом электрода и получены количественные данные. [38]
С Г, осложненный, по-видимому, параллельным разрядом HgO, на котором отражается полупроводниковая природа поверхностного окисла, в частности, локализация части общего скачка потенциала в объемном заряде. [39]
Изменение лимитирующей стадии процесса при переходе от кислых рает-воров к щелочным связано с изменением каталитических свойств кислого поверхностного окисла серебра. [40]
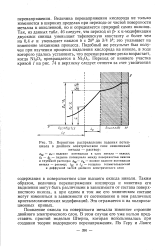 |
Вероятное распределение падения потенциала в двойном электрическом слое окисленный. [41] |
Таким образом, величина перенапряжения кислорода и кинетика его выделения могут быть различными в зависимости от состава поверхностного окисла, а при одном и том же его химическом составе могут изменяться в зависимости от соотношения в нем различных кристаллохимических модификаций. Это отражается и на поляризационных кривых. [42]
С позиций стадийности окислительно-восстановительного катализа в работах Г.К. Борескова и его сотрудников последовательно развивалась концепция об энергии связи кислорода поверхностного окисла как факторе, существенно определяющем активность катализатора в реакциях окисления органических веществ. [43]
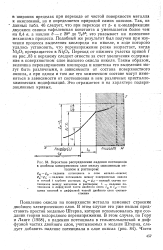 |
Вероятное распределение падения потенциала в двойном электрическом слое между окисленным металлом и раствором. [44] |
Таким образом, величина перенапряжения кислорода и кинетика его выделения могут быть различными, в зависимости от состава поверхностного окисла, а при одном и том же его химическом составе могут изменяться в зависимости от соотношения в нем различных кристалло-химических модификаций. Это отражается и на характере поляризационных кривых. [45]
Страницы: 1 2 3 4