Окисление - изобутан
Cтраница 3
В качестве примера на рис. 132 приведены кинетическая кривая накопления гидроперекиси и измеряемый указанным способом разогрев для реакции окисления изобутана. Видно, что на первом этапе процесса, когда основным химическим процессом является накопление гидроперекиси, имеется хорошее соответствие между обеими кривыми. В частности, точке перегиба на кривой накопления гидроперекиси соответствует точка максимума на кривой разогрева. [32]
Следует признать странным подобное утверждение со стороны авторов, почти одновременно экспериментально установивших, что разветвляющим агентом при окислении изобутана является ацетальдегид, а никак не перекись [12] ( см. стр. Такое противоречие вызвано, очевидно, тем, что авторы не находят иного пути образования ацетона при окислении изобутана, кроме как распадом трет, бутокси-радикала. На самом же деле вполне возможно предположить иной путь образования ацетона и притом нисколько не противоречащий современным представлениям о механизме окисления нормальных парафиновых углеводородов. [33]
В результате парофазных реакций гидроперекиси выделить не удается, она была выделена в результате жидкофазных; например, при окислении изобутана удалось выделить в качестве промежуточного продукта гидроперекись трет-бутнла. В системах, в которых отсутствует легко отщепляемый атом водорода, разложение перекисного радикала может протекать по-разному. [34]
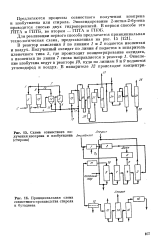 |
Схема совместного по.| Принципиальная схема совместного производства стирола и бутадиена. [35] |
В реактор окисления 3 по линиям 1 и 2 подаются изопентан и воздух. Окисление изобутана ведут в реакторе 10, куда по линиям 8 и 9 подаются углеводород и воздух. [36]
Наиболее перспективный метод получения третп-бутилгидроперекиси - окисление изобутана в сжиженном состоянии. При окислении изобутана в растворе инертных веществ [15-17] в присутствии солей кобальта переменной валентности была получена широкая гамма продуктов окисления деструктивного характера, в том числе только следы трет-бу-тилгидроперекиси. [37]
Первичные и вторичные алканы при этом дают главным образом кислоты и кетоны, а третичные являются, в основном, источником перекисей. Так, окисление изобутана при 158 С и 3 мин контакта дает 42 % ди-грег-бутиллерекиси наряду с грег-бутанолом и некоторым количеством изомасляного альдегида; изменение условий реакции приводит к образованию 75 % трет-бутилгидропере-кнси. [38]
Первичные и вторичные алканы при этом дают главным образом кислоты и кетоны, а третичные являются, в основном, источником перекисей. Так, окисление изобутана при 158 С и 3 мин контакта дает 42 % ди-грег-бутилперекиси наряду с грег-бутанолом и некоторым количеством изомасляного альдегида; изменение условий реакции приводит к образованию 75 % трет-бутилгидропере-кнси. [39]
При эпоксидировании пропилена трет-бутилгидропероксидом сырьем являются пропилен и изобутан. Грет-бутилгидропероксид получается окислением изобутана при 120 - 130 С и 3 0 - 5 0 МПа. Эпоксидирование пропилена грег-бутилгидропероксидом осуществляется при 130 С и 2 - 4 МПа в присутствии катализатора. [40]
При анализе растворов гидроперекисей влияние воды можно избежать, используя нечувствительный к воде детектор. Например, анализ продуктов окисления изобутана ( метанол, ацетон, третичный бутиловый спирт, ди-грея-бутшше-рекись и гидроперекись третичного бутила) на хроматографе с катарометромзэ может быть осуществлен на составной колонке общей длиной 2 7 м за 64 мин. Анализ тех же продуктов на приборе с лламеино-ионизационным детектором занимает 15 - 20 мин. [41]
При анализе растворов гидроперекисей влияние воды можно избежать, используя нечувствительный к воде детектор. Например, анализ продуктов окисления изобутана ( метанол, ацетон, третичный бутиловый спирт, ди-трея-бутилпе-рекись и гидроперекись третичного бутила) а хроматографе с катарометром35 может быть осуществлен на составной колонке общей длиной 2 7 м за 64 мин. Анализ тех же продуктов на приборе с пламенно-ионизационным детектором занимает 15 - 20 мин. [42]
Разложение ГПТБ мы изучали в окисляющемся изопентане, а ГПТА в окисляющемся изобутане, полагая, что по своим характеристикам эти углеводороды близки и замена одного другим не вызовет принципиального изменения протекающих процессов. Кроме того, было проведено окисление изобутана и изопентана в присутствии собственных гидроперекисей. [43]
Количественное определение продуктов реакции по ИК-полосам поглощения их в газовой фазе может быть осложнено тем, что оптическая плотность изменяется нелинейно с давлением. Такой прием был использован при изучении реакции окисления изобутана в газовой фазе в присутствии бромистого водорода. [44]
Из этана в этих условиях была получена уксусная кислота, из пропана-ацетон и некоторое количество пропионовой кислоты. Окисление н-бутана приводило к образованию метилэтилкетона и диацетила; продуктами окисления изобутана были гидроперекись трсш-бутила и / / wn - бутиловый спирт. Выход полезных продуктов составлял около 50 - 80 %, считая на прореагировавший углеводород. Перекись mpem - бутила, получаемую таким способом, применяют в США в качестве катализатора для реакций полимеризации. [45]
Страницы: 1 2 3 4
