Окисление - катион
Cтраница 2
Из этого уравнения следует, что и для реакции окисления катионов аналогично реакции восстановления анионов первой группы поляризационная кривая в разбавленных растворах имеет сложную форму с максимумом тока при qG и минимумом при 70, причем скорость реакции зависит от о - потенциала, величина и знак которого определяются составом раствора и потенциалом электрода. [16]
ПАОВ на кинетику восстановления анионов и катионов, а также окисления катионов i-эффект зависит от знака заряда реагирующей частицы, а потому дает информацию о механизме действия этих ПАОВ на скорость разряда - ионизации. [17]
В работах Н. В. Николаевой-Федорович рассмотрено влияние адсорбированных ПАВ на реакции восстановления анионов и окисления катионов. Результаты, полученные в этих и некоторых других исследованиях, полностью подтверждают электростатический характер действия ПАВ на кинетику реакции восстановления. Рассматривая влияние Wi потенциала на скорость реакции, следует заметить, что основная часть ионов расположена во внешней плоскости Гельмгольца и в диффузном слое, однако имеется некоторое количество ионов, которые находятся во внутренней области Гельмгольца и непосредственно соприкасаются с поверхностью электрода. Было показано, что именно эти ионы и участвуют в разряде. [18]
Перейдем к реакциям между бинарными кристаллами, каждый из которых склонен изменять степень окисления катионов. [19]
Добавление щавелевой кислоты к серно - или уксуснокислому раствору приводит к уменьшению степени окисления катиона, содержащего полоний, который характеризуется тем же потенциалом, что и потенциал, наблюдаемый в чистой щавелевой кислоте. Выделение на аноде прекращается. [20]
В комплексах, в состав которых входят катионы в низшем валентном состоянии, возможно окисление катиона до высшего валентного состояния. [21]
Суммарный заряд многогранника равен ( и - 2с) е, где v - степень окисления катиона, с - координационное число. [22]
Суммарный заряд многогранника равен ( v - 2с) е, где v - степень окисления катиона, с - координационное число. [23]
Окислы железа8 11 13 61, хрома8 11, меди8 - и, в которых степень окисления катиона легко изменяется в ходе реакции, индуцируют побочные реакции деструктивного окисления кислот, способствуют образованию альдегида - продукта восстановления кислоты и приводят к появлению в газообразных продуктах СО, Н2, предельных и непредельных углеводородов. [24]
Атомная масса металла А - Э - х, причем 1 х 4 ( в солях степень окисления катиона не превышает 4), и имеет целочисленное значение. [25]
Каков бы ни был механизм, для активных центров катализаторов наиболее вероятны обратимые изменения координации без изменения степени окисления центрального катиона. Одновременное изменение координационного числа и степени окисления, вероятно, связано с более значительными изменениями ЭСКП. [26]
Поскольку окислительно-восстановительные свойства могут иметь как катионы, так и анионы, то на одной колонке можно получить хроматограммы продуктов окисления катионов и анионов, в соответствии с их способностью к окислению - восстановлению. [27]
Поскольку окислительно-восстановительные свойства могут иметь как катионы, так и анионы, то на одной колонке можно получить хро-матограммы продуктов окисления катионов и анионов, в соответствии с их способностью к окислению - восстановлению. [28]
Поскольку окислительно-восстановительные свойства могут иметь как катионы, так и анионы, то на одной колонке можно получить хроматограммы продуктов окисления катионов и анионов, в соответствии с их способностью к окислению - восстановлению. [29]
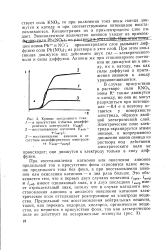 |
Кривые предельного тока. [30] |
Страницы: 1 2 3 4