Окисление - олефин
Cтраница 1
Окисление олефинов, а также парафинов и ароматических углеводородов на окислах и металлах показано преобладание параллельного независимого образования различных продуктов окисления - окисей, спиртов, альдегидов, кислот, углекислого газа и СО. Каждая последовательность процессов совершается с определенным экземпляром молекулы и обрывается при образовании устойчивого продукта, способного уйти в объем. [1]
Окисление олефинов в крупных масштабах в промышленности осуществляется для получения окисей олефинов, альдегидов, непредельных альдегидов и спиртов, например акролеина и аллилового спирта. Окисление некоторых олефинов может привести к разнообразным кетонам. [2]
Окисление олефинов раствором пермангапата приводит к расщеплению двойной связи с получением карболовых кислот. Как показал еще Вапгер [255], при этом образуются в качестве промежуточных продуктов гликолп. [3]
Окисление олефинов, катализируемое солями палладия. [4]
Окисление олефинов может протекать по следующим схемам. [5]
Окисление олефинов перекисными соединениями сопровождается образованием эпоксидных или гидрокси-лированных соединений. [6]
Окисление олефинов до альдегидов является реакцией р-типа, а их дальнейшее окисление - реакцией л-типа. Присутствие небольших количеств элементов с электроотрицательностыо большей, чем у меди, модифицирует поверхность, изменяя распределение указанных двух типов центров и, тем самым, скорость и селективность процесса. [7]
Окисление олефина хромовой кислотой обычно проводится в растворах уксусной кислоты, уксусного ангидрида или серной кислоты, и проходит оно труднее, чем окисление первичного или вторичного спирта. Эти процессы окисления катализируются кислотой и поэтому включают смешанные ангидриды или, вероятно, катион ( НСгО3) е, в котором электроноакцептор-ные свойства связи Сг О увеличены благодаря положительному заряду. [8]
Окисление олефинов перманганатом совершенно отлично по природе, так как его можно проводить в нейтральном или щелочном растворе или в таких растворителях, как ацетон и пиридин. В нейтральном или слабокислом растворе перманганат немедленно превращает олефин в ацилоин, причем довольно трудно задержать дальнейшее окисление; однако в достаточно щелочном растворе при рН 12 ( или более) окисление в основном останавливается на стадии образования цис -, 2-диола. В деталях механизм реакции выяснен Уибергом, который принял во внимание тот факт, что перманганат, меченный 180, не обменивает своих кислородных атомов с водой, но все же окисляет олеат с переходом меченого кислорода к органическим продуктам реакции. Эта работа подтверждает ранее высказанные предположения, что при окислении перманганатом происходит образование пятичленного циклического аддукта ( XXXVI), который затем гидролизуется с расщеплением Мп-О - связи. [9]
Окисление олефина до двузамещенной перекиси определяется теми же тремя стадиями. [10]
Окисление олефинов по ненасыщенному атому углерода с образованием карбонильных соединений, не сопровождающееся деструкцией углеводородной цепи, представляет не только теоретический, но и большой практический интерес. [11]
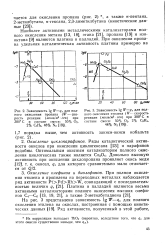 |
Зависимость lg W - qs для полного окисления пропана ( W - ско.| Зависимость lg W - qs для полного окисления этилена ( W-скорость. [12] |
Окисление олефинов и диолефинов. [13]
Окисление олефинов перекисными соединениями сопровождается образованием эпоксидных или гидрокси-лированных соединений. [14]
Окисление олефинов раствором перманганата приводит к расщеплению двойной связи с получением карбоновых кислот. Как показал еще Вагнер [255], при этом образуются в качестве промежуточных продуктов гликоли. [15]
Страницы: 1 2 3 4