Окисление - этилбензол
Cтраница 1
Окисление этилбензола в жидкой фазе хромовой смесью, марганцовокислым калием или иными окислителями ведет к образованию лишь бензойной кислоты, но в особых условиях можно окислить только СН2 - группу и получить ацетофенон. Последний получают обычно из бензола с хлористым ацетилом в присутствии А1С13, но новейшие каталитические методы удобнее и цроще. [1]
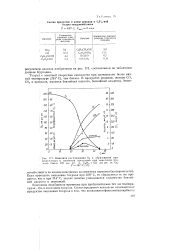 |
Кинетика расходования О2 и образования промежуточных и конечных продуктов при окислении бен -. г.ола. Смесь 225 мм рт. ст. C ( jH0 - - 425 мм рт ст Q2 - Т 487 С [ 17. [2] |
Окисление этилбензола протекает при приблизительно тех же температурах, ч [ го и окисление толуола. [3]
Окисление этилбензола и кумола при соотношении термофилов и мезофилов 1: 4 протекало в 40 раз медленней, чем окисление алканов и нафтенов ( см. табл. 4.2), а - окисление циклогексана и циклогексена в 100 - 125 раз медленней. Изменение ХПК и БПКПОЛН сточных вод, содержащих ароматические углеводороды, окисление сульфидов до сульфатов, накопление углерода, а также биомассы бактерий в активном иле происходит в 1 5 - 2 раза медленнее. [4]
Окисление этилбензола в жидкой фазе хромовой смесью, марганцовокислым калием или иными окислителями ведет к образованию лишь бензойной кислоты, но в особых условиях можно окислить только СН2 - группу и получить ацетофенон. Последний получают обычно из бензола с хлористым ацетилом в присутствии А1С13, но новейшие каталитические методы удобнее и проще. [5]
Окисление этилбензола осуществляется при избытке подаваемого воздуха, обеспечивающего необходимую концентрацию рас-творенного кислорода в жидкой фазе, что требует проведения процесса под давлением при температуре 130 - 160 С. [6]
Окисление этилбензола до гидропероксида проводится обычно в каскаде реакторов барботажного типа при 140 - 150 С и давлении 0.3 - 0.5 МПа в присутствии ионов щелочных металлов. [7]
Реакцию окисления этилбензола проводили в периодическом реакторе идеального смешения при температуре 120 С, расход кислорода составлял 0 6 л / мин. [8]
Скорость окисления этилбензола в области концентрации Со3 ( 3 0 - 3 6) - 10 - 4: 1 5Х ХЮ-2 моль / л практически не меняется. При большей концентрации Со3 реакция заметно замедляется. [9]
При окислении этилбензола получаются гидроперекись, метилфенил-карбкнол и ацетофенон. [10]
При окислении этилбензола в присутствии ацетата кобальта и различных ингибиторов при температурах 50 - 90 С и концентрациях ацетата кобальта, превышающих ( 5 - 10) - 10 - 3 молъ / л, уже через 2 - 3 мин. [12]
Изучение кинетики окисления этилбензола в присутствии аминов и фенольных соединений [5] показало, что в процессе окисления концентрация амина в смеси остается постоянной вплоть до полного расходования фенола. Это, вероятно, связано с тем, что при окислении амина образуется свободный радикал, который отрывает атом водорода от молекулы фенола, давая новую молекулу амина; вследствие этого концентрация амина практически не меняется до тех пор, пока не израсходуется весь фенол. [13]
Основной продукт окисления этилбензола - вторичный спирт ( метилфенилкарбинол), который подвергается окислению до бенз-альдегида. Первичный спирт образуется лишь в незначительных количествах. Образование бензальдегида начинается только после окисления почти всего углеводорода до спирта. [14]
Изучение кинетики окисления этилбензола в присутствии аминов и фенольных соединений52 показало, что в процессе окисления концентрация амина в смеси остается постоянной вплоть до полного расходования фенола. Это, вероятно, связано с тем, что при окислении амина образуется свободный радикал, который отрывает атом водорода от молекулы фенола, давая новую молекулу амина; вследствие этого концентрация амина практически не меняется до тех пор, пока не израсходуется весь фенол. [15]
Страницы: 1 2 3 4