Последующее окисление
Cтраница 3
Такое погружение с последующим окислением называется проходом. [31]
Гидроборирование 1-фенилциклогексена с последующим окислением промежуточно образующегося борана перекисью водорода приводит к соединению, структура которого, как можно ожядать, должна быть. [32]
Положение двойной связи осложняет последующее окисление этого производного посредством реакций р-окисления. Полученное соединение имеет двойную связь в р у-положении вместо - положения, как требуется для нормального Р - окисления. Однако неблагоприятное расположение двойной связи может быть изменено под действием еноилгидразы ( еноил - КоА - гидратазы), которая превращает р у-ненасыщенные производные ацил - КоА ва р-ненасыщенные соединения. Вторая двойная связь в линолевой кислоте, расположенная между 12 - м и 13 - м углеродными атомами, переходит в нормальное а р-положение, требуемое для р-окисления. Третья двойная связь в линолевой кислоте между 15 - м и 16 - м углеродными атомами также находится в неподходящем для р-окисления положении и требует действия еноилгидразы как изомеразы положения. Следовательно, теоретически возможно посредством реакций Р - окисления расщепить олеиновую, линолевую и линоленовую кислоты при использовании еноилгидразы как изомеразы положения. [33]
Механизм разряда дырок и последующее окисление антрацена в ант-рахинон возле водного выходного электрода еще до конца не изучены. [34]
Поскольку реакции сульфидирования и последующего окисления протекают главным образом в головном ящике, необходимо периодически переключать ящики для поддержания требуемого распределения серы и влаги во всех ящиках. Если в цепочке имеются п ящиков, то номер каждого ящика в цепочке последовательно переключается от первого к / г-ому. [35]
Гидрирование, обычно с последующим окислением. [36]
Гидроборирование несимметричных алкенов с последующим окислением H2U2 позволяет установить региоспецифичностъ и стереоспецифичность всего процесса. Так, например, при гидроборировании 1-метилциклогексена с последующим окислением триалкилборана щелочным раствором перекиси водорода образуется трзнс-2 - метилциклогексанол. Это означает, что при окислении группа BR2 замещается на гидроксил с полным сохранением геометрической конфигурации. Направление гидратации алкена в этом двухстаднйиом процессе полностью противоположно региоселективности прямой гидратации алкенов или региоселективности оксимеркурирования - демеркурирования алкенов ( разд. [37]
Михлера с фенил-а-нафтилами-ном и последующим окислением или, предпочтительно, конденсацией кетона Михлера с фенил-а-нафтиламином в присутствии хлорокиси фосфора. Последний метод является основным способом получения таких трифенилметановых красителей. Кетон Михлера выделять необязательно; два моля диметиланилина или диэтиланилина ( применяют 35 % - ный избыток, который потом регенерируют) конденсируют с фосгеном в присутствии хлористого цинка в кетон, добавляют растворитель ( например, толуол) и вторую стадию реакции проводят добавляя 1 моль соответствующего амина и хлорокись фосфора. Первую стадию - фосгенирование - проводят медленно, в течение нескольких дней при постепенном повышении температуры. После частичной нейтрализации едким натром отгоняют толуол; краситель выделяется в виде смолы, из которой примеси удаляют обработкой ксилолом, а дальнейшую очистку проводят растворением в соляной кислоте и высаливанием. [38]
При дегидратации, с последующим окислением хромовой кислотой первый диол дает Ce-дикетон, а второй Св - дикие лоту. [39]
На этой реакции и последующем окислении N0 в NO2 и абсорбции двуокиси азота водой основаны промышленные способы производства азотной кислоты. [40]
На этой реакции и последующем окислении NO в NO2 и абсорбции двуокиси азота водой основаны промышленные способы производства азотной кислоты. [41]
Превращение сульфохлорида в сульфоксид и последующее окисление [304] ведут к образованию соответствующей карбоновой кислоты, как и в случае [ 3-сульфохлорида. [42]
Конденсация о-толуидина с формальдегидом и последующее окисление полученного бис ( 4-амино - З - метилфенил) метана. [43]
Превращение сульфохлорида в сульфоксид и последующее окисление [304] ведут к образованию соответствующей карбоновой кислоты, как и в случае р-сульфохлорида. [44]
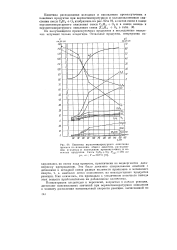 |
Кинетика верхнетемпературного окисления пропана по изменению общею давления, расходованию исходных и накоплению промежуточных и конечных продуктов. Смесь С3Н8 С2. PHSL4 282 мм рт. ст.. Г 350 С. [45] |
Страницы: 1 2 3 4