Окись - дейтерий
Cтраница 1
Окись дейтерия является промышленным продуктом и доступна в больших количествах; ее используют в качестве замедлителя в ядерных реакторах, поскольку она очень эффективно понижаетэнер-гию быстрых нейтронов ядерного деления до энергии тепловых нейтронов, а также вследствие того, что дейтерий имеет гораздо меньшее сечение захвата нейтронов, чем водород, и, следовательно, заметно не уменьшает нейтронный поток. Дейтерий широко применяют при изучении механизмов реакций и при спектроскопических исследованиях. [1]
 |
Приближенная модель скелетных валентных колебаний полипропилена. [2] |
Реакция целлюлозы с окисью дейтерия была изучена Манном и Марри-наном [6, 32], а также рядом других авторов. Реакция дейтерирования вискозной пленки ( целлюлоза II) парообразной D2O вначале протекает очень быстро. По истечении 5 мин наблюдается существенное уменьшение поглощения в области 3600 - 3000 см 1, связанного с валентными колебаниями групп ОН, и появляется новая широкая полоса в области 2700 - 2400 см 1, характерная для валентных колебаний групп OD. Процесс дейтерирования продолжается до тех пор, пока ( примерно через 1 час) широкая полоса поглощения групп ОН полностью не исчезнет; в спектре при этом остается четыре хорошо разрешенных полосы, характеризующих валентные колебания групп ОН в кристаллических областях. Скорость реакции дейтерирования и глубина ее при проведении процесса в жидкой фазе выше, чем в парообразной. [3]
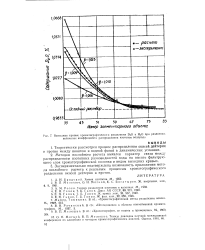 |
Выходные кривые хроматографическою разделения D2O и Н2О при различных величинах коэффициента распределения изотопов водорода. [4] |
Теоретически рассмотрен процесс распределения окисей дейтерия и протия между ионитом и водной фазой в динамических условиях. [5]
Обработка таких литиевых производных окисью дейтерия дает HRe ( n - CsH4D) 2 или Н2М ( я - С5Н4О) 2, связи металл - водород остаются неизменными. [6]
При обработке этих солей окисью дейтерия происходит дейте-рообмен, в результате чего образуются амиды с высоким содержанием дейтерия, связанного как с атомом азота, так и с а-угле-родным атомом. Очевидно, что подобно D2O с нитрилами могут реагировать также другие изотопные разновидности воды. [7]
Исследования реакции обмена между окисью дейтерия и целлюлозой проводились давно, однако лишь в последние годы эту реакцию стали применять для характеристики структуры целлюлозы. Первые попытки изучения реакции [1-3] были сопряжены с экспериментальными трудностями, которые заключались в быстром протекании реакции обмена с атмосферной влагой. Эти трудности были преодолены только в 1948 г. [4], когда появилось первое правильное описание скорости и степени протекания этой реакции. [8]
 |
Подвижность ионов при 25 С. [9] |
Сюда же включены данные для окиси дейтерия. [10]
Обычно вода содержит малые количества окиси дейтерия D2O - химического индивидуума, по свойствам очень близкого к Н2О, но содержащего тяжелый изотоп водорода. Окись дейтерия образуется не из Н2О, и поэтому обыкновенная вода не является, строго говоря, однокомпонентной системой; но поскольку D2O присутствует в этой воде в очень малой концентрации, являющейся к тому же постоянной, то для практических целей обыкновенную воду можно считать системой однокомпонентной. [11]
 |
Температурная зависимость коэффициента разделения ( К ( крк-вая 1 и различия в растворимости хлористого калия в НаО и DjO ( кривая 2. [12] |
Как видно, абсолютное содержание окиси дейтерия в равновесном с ио-нитом растворе увеличивается по мере повышения концентрации D20 в исходном растворе. Этого и следовало ожидать, поскольку растворяющая способность растворов тяжелой воды уменьшается линейно с увеличением содержания дейтерия. В наших опытах это обусловливает предпочтительную сорбцию молекул легкой воды полярными группами ионита. [13]
Иногда реакцию металлоорганических соединений с окисью дейтерия используют для введения дейтерия в молекулы органических соединений. [14]
Как видно из графиков, содефжание окиси дейтерия убывает с уменьшением количества воды, остающейся в смоле. Следовательно, в гидратных оболочках активных групп смолы и нейтрализующих их ионов происходит градиентное распределение D20, концентрация которой уменьшается по направлению от периферии к твердой фазе смолы вследствие меньшей энергии связи D20 с полярными группами ионита. [15]
Страницы: 1 2 3 4