Окись - дейтерий
Cтраница 2
Получена обменом обычной фосфорноватистой кислоты в разбавленной окисью дейтерия в течение длительного времени ( 2 - 3 суток) при комнатной температуре. [16]
Как и следовало ожидать, вода и окись дейтерия сходны по кислотно-основному поведению. Обратимый к ионам дейтерия, газовый дейтериевый электрод легко получается на платиновой поверхности, погруженной в тяжелую воду. Диэлектрические постоянные окиси дейтерия и воды весьма близки ( 77 9 для окиси дейтерия и 78 4 для воды при 25 С), тогда как плотность тяжелой воды ( 1 1 г / мл при 25 С) на 10 % выше плотности обычной воды. [17]
Растворы для калибровки градиентов приготовляют путем разбавления окиси дейтерия ( желательна чистота большая, чем 99 9 %), тщательно очищенной обычной водой. [18]
Исследованию обмена водорода между органическими соединениями и окисью дейтерия DoO, тяжелым этиловым спиртом C2HsOD, тяжелым аммиаком ND3 и тяжелыми кислотами посвящено много сотен сабот. Все имеющиеся в литературе данные по этому вопросу собраны и табл. 14, 15 и 17, а важнейшие выводы из опытного материала, теоретические представления и обобщения рассмотрены ниже. [19]
Вода, состоящая из дейтерия и О16 ( окись дейтерия), носит название тяжелой, так как она на 10 77 % тяжелее обычной воды. В отличие от большинства изотопических близнецов, совсем нетрудно различить по физическим свойствам эти два идентичных соединения, различающихся лишь стабильными изотопами одного элемента. Так, вязкость тяжелой воды на 23 2 %, точка плавления на 3 81, точка кипения на 1 43 больше, чем у обычной воды; последняя, как правило, лучше растворяет соли, чем тяжелая вода. Все это объясняется тем, что масса дейтерия вдвое больше массы протия. [20]
Наблюдаемое отношение констант скоростей в чистой воде и окиси дейтерия / Сн2сДо2о равно ( & H / & D) i ( & H / D) H где ( / cH / & D) n - вторичный изотопный эффект. Вторичный изотопный эффект отражает изотопные различия в частотах и нулевых энергиях связей с атомами, которые не переносятся в переходном состоянии, например различия между переходными состояниями X и XI. [21]
Вода тяжелая ( 2Н2О или D20) - окись дейтерия, химическое соединение изотопа водорода дейтерия с кислородом. Используется как замедлитель нейтронов и теплоноситель в атомных реакторах и для приготовления меченых соединений, используемых в качестве радиоактивных индикаторов. [22]
Остается выяснить, какая каталитическая реакция ослабляется введением окиси дейтерия. [23]
Кроме того, имеется еще метод определения количества окиси дейтерия в воде, основанный на разности в давлении пара для легкой и тяжелой формы ( Райц и Бонгеффер 1935 г.) водорода. [24]
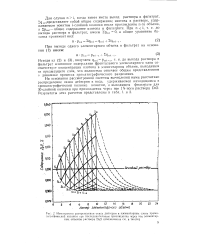 |
Номограмма распределения окиси дейтерия в элементарных слоях хрома-тографической колонки при последовательном прохождении через нее элементарных объемов раствора D2O ( обозначения в тексте. [25] |
На основании рассмотренной системы вычислений нами рассчитано распределение окиси дейтерия в воде, удерживаемой находящимся в хроматографической колонке ионитом, и выходящем фильтрате для 30-слойной колонки при прохождении через нее 1 % - ного раствора DzO. [26]
Метан обменивается с полностью дейтерированным метаном, с окисью дейтерия и с самим дейтерием. Для получения дейтерометанов с различной степенью замещения можно использовать целый ряд катализаторов-металлов, в частности металлы, относящиеся к группе переходных. [27]
Изучая реакцию дейтеро-обмена между n - ксилолом и окисью дейтерия, катализируемую никелем, Хирота, Кувата и Уеда [254] нашли, что атомы водорода метальных групп n - ксилола обмениваются с дейтерием легче, чем атомы водорода бензольного кольца. [28]
Гидроксильные группы на поверхностях окислов легко обмениваются с окисью дейтерия, образуя дейтероксильные группы. [29]
Вода, состоящая из молекул D20 и называемая окисью дейтерия, или тяжелой водой, получила применение в качестве замедлителя в ядерных котлах ( стр. Она медленнее подвергается электролизу, чем обычная вода. Этим пользуются для ее выделения. Особенность тяжелой воды как растворителя та, что в ней сильно снижена активность ферментов. Благодаря этому она как бы подавляет процессы в живых организмах, выступая в роли своеобразного яда. [30]
Страницы: 1 2 3 4