Окись - дейтерий
Cтраница 3
То, что наблюдаемый изотопный эффект реакции бензол - окись дейтерия при 30 составляет 1 7 0 1 [38], показывает, что в рамках диссоциативного механизма л-комплексного замещения эта реакция является стадией, контролирующей скорость процесса. Полученный результат согласуется с прямыми наблюдениями других исследователей [41, 42], которые показали, что хемосорбция ненасыщенных углеводородов происходит с большей скоростью, чем их последующее взаимодействие с хемосорбированным водородом. [31]
Изотопные эффекты в ферментативных реакциях, которые проводят в окиси дейтерия, нельзя интерпретировать строго, хотя из данных достаточно детального исследования можно с различной степенью уверенности сделать определенные выводы. Прежде всего наобходимо определить, насколько наблюдаемый изотопный эффект отражает изменения характеристик различных ионогенных форм фермента или субстрата при замене воды на окись дейтерия. Желательна проверка этой процедуры непосредственным сравнением показаний рН - метра, полученных с 0 001М НС1 в воде и с 0 001М DC1 в окиси дейтерия. Различие в константах ионизации субстрата в воде и в окиси дейтерия можно определить непосредственно; соответствующее различие активных форм фермента можно обнаружить лишь из зависимости ферментативной активности от рН ( или pD), либо путем изучения изотопного влияния на кислотность ионогенных групп, о которых известно, что они важны для проявления ферментативной активности. [32]
Исторически следующим и наиболее широко распространенным сейчас методом концентрирования окиси дейтерия в воде является процесс электролиза; он применяется в промышленном масштабе для получения тяжелой воды. Условия электролиза не ограничены строго - можно употреблять любой электродный материал за исключением, пожалуй, платинированной платины, а электролит может быть щелочным или кислым. [33]
ШО и D2O 151, уменьшается с ростом содержания окиси дейтерия в исходной смеси. Следовательно, молекулы HzO проникают через мембрану в большем количестве, и продиффундировавшая доля смеси частично обогащена окисью протия. При переходе от калиевой к натриевой и затем литиевой формам протекаемость мембраны увеличивается по отношению ко всем изотопным формам. Последняя, как и в случае гранулированных сульфокатио-нитов [8], возрастает с увеличением энергии гидратации насыщающего иона. [34]
Кривая 1 этого рисунка показывает, что с помощью окиси дейтерия можно заместить на дейтерий почти все атомы водорода структурной воды катализатора. [35]
Метан обменивается с метаном - dj, дейтерием и окисью дейтерия; скорости при 184 С убывают в данной последовательности. Кажется ясным, что метан хемосорбируется при разрыве С - Н - связи. Энергия активации 19 ккал для обмена с метаном-с относится к энергии десорбции метана. Более медленная реакция с дейтерием имеет энергию активации 28 ккал, и более медленная скорость приписывается тому, что дейтерий сильно адсорбируется и вытесняет метан с поверхности. [36]
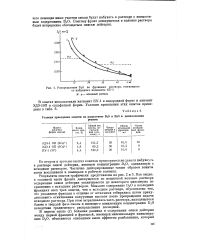 |
Распределение DzO во фракциях раствора, отогнанного от набухшего катионита КУ-1. [37] |
Поэтому фронт движущегося в колонке раствора будет непрерывно обогащаться окисью дейтерия. [38]
Гораздо большая скорость и глубина обмена алюмосиликатного катализатора с окисью дейтерия по сравнению с дейтерием, как уже указано выше, обусловлена, вероятно, ослаблением связи водорода с кислородом воды за счет смещения электронов кислорода к алюминию при хемоеорбции воды на прокаленном алюмосиликатом катализаторе. Это позволяет предположить, что скорость - обмена различных углеводородов с дейтерированным алюмосиликатным катализатором будет расти с усилением тенденции к смещению электрона от атома водорода к атому углерода в молекуле углеводорода, находящейся на активном центре катализатора. [39]
Таким же способом можно легко анализировать состав растворов воды и окиси дейтерия, наблюдая смешиваемость раствора с 3-пиколином. [40]
Примером изотопного обмена является обмен между обычной молекулой воды и окисью дейтерия. [41]
На основании температурной зависимости скорости этой реакции в обычной воде и окиси дейтерия при ионной силе 1 были рассчитаны термодинамические величины активации. [42]
Изолированное наблюдение различия скорости ферментативно катализируемой реакции в воде и в окиси дейтерия не дает ничего существенного для понимания механизма реакции. Элементарные требования, необходимые для интерпретации изотопных эффектов в ферментативных реакциях, заключаются в следующем: 1) необходимо разделение влияний изотопного замещения на максимальную скорость и на - йГщ с дальнейшим разделением влияний на элементарные константы скоростей и равновесий реакции; 2) необходимо разграничение изотопных эффектов для водородных атомов, необменивающихся и быстро обменивающихся с растворителем; 3) для экспериментов, проводимых в растворах окиси дейтерия, необходимо определение влияния этого растворителя на зависимость максимальной скорости и константы Михаэлиса от кислотности. Изотопные эффекты в реакциях переноса необменивающихся атомов водорода, которые обычно связаны с углеродом, интерпретировать относительно легко, поскольку их можно изучать в растворителе постоянного состава, в то время как протоны, связанные с кислородом, азотом или серой, всегда обмениваются с растворителем с диффузионно контролируемой скоростью, которая много выше, чем у изучаемой реакции; дейтериевый изотопный эффект в таких реакциях необходимо изучать при использовании окиси дейтерия в качестве растворителя, что влечет за собой определенные трудности в интерпретации результатов, связанных с влиянием растворителя. [43]
Далее, когда дейтерооксибромид алюминия, приготовленный таким же образом из окиси дейтерия и бромистого алюминия, применялся в качестве катализатора, изомеризация к-бутана протекала с очень небольшим дейтеро-во-дородным обменом. [44]
Во втором и третьем опытах ионитам предварительно давали набухнуть в растворе окиси дейтерия, имевшем концентрацию D20, одинаковую с исходным раствором. Частично дейтерированные таким образом иониты затем высушивали и помещали в рабочую колонку. [45]
Страницы: 1 2 3 4