Адсорбированная окись - углерод
Cтраница 1
Адсорбированная окись углерода изменяется в ионном проекторе значительно меньше, чем кислород. В отличие от азота СО, вероятно, занимает плоскости 110 даже при комнатной температуре. Это говорит ве только о существенном различии во влиянии поверхностной структуры на различные молекулы / но также свидетельствует о том, что появление индивидуальных центров эмиссии не служит доказательством их химического строения. [1]
ИК-спектры адсорбированной окиси углерода говорят о существовании двух ее форм [22, 23], одна из которых ( мостико-вая) включает два поверхностных атома металла, а другая ( линейная) - один такой атом. [2]
При окислении адсорбированной окиси углерода должен получаться бидентатный комплекс М - О - О СО-МО - ОСО, который затем должен давать углекислый газ, возможно, через стадию образования относительно стойкого карбонат-иона. [3]
СО) обозначает адсорбированную окись углерода. [4]
Когда экспериментальные значения частот карбонила адсорбированной окиси углерода были нанесены на гиперболическую кривую, то оказалось, что число валентных электронов в поверхностных соединениях - дробная величина. Предполагалось, что эти дробные части характерны для каждого металла. [5]
В ИК-спектре цеолита AgA с адсорбированной окисью углерода при давлении 300 мм рт. ст. и комнатной температуре в области 2000 - 2200см 1 наблюдается сильное поглощение, которое следует отнести к молекулам окиси углерода, как адсорбированным на поверхности, так и находящимся 50 в мертвом пространстве кюветы. [6]
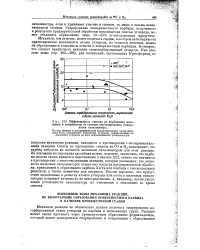 |
Эффективность синтеза по карбидному механизму в зависимости от степени карбидирования поверхности катализатора. 1. [7] |
Механизм реакции не обязательно должен включать гидрирование адсорбированной окиси углерода до карбида и метиленовых групп. [8]
Полоса при 4 85 мкм, приписанная линейной форме адсорбированной окиси углерода, на палладии относительно слаба, а на биметаллических катализаторах становится преобладающей. Две другие полосы, приписанные мостиковой форме окиси углерода, очень слабы в спектрах биметаллических катализаторов. Объясняется такая зависимость следующим образом: два рассматриваемых металла, как и можно было ожидать, образуют сплав. Очевидно, что это существенно отличается от того случая, при котором частицы сплава не образуются. [9]
За исключением полос поглощения при 2060 и 1950 см 1, принадлежащих адсорбированной окиси углерода, все полосы, представленные в табл. 9, исчезали при откачке газовой фазы. Поэтому эти полосы поглощения следует рассматривать как полосы газовой фазы или как полосы поглощения очень слабо связанных поверхностных соединений. Никаких стабильных соединений, помимо адсорбированной окиси углерода, не было обнаружено. [10]
Было предложено также и другое объяснение природы высокочастотных полос поглощения в спектре адсорбированной окиси углерода. Поверхностные соединения, дающие эти полосы поглощения, Гарднер и Петруччи ( 1960, 1961) рассматривали в частично или полностью ионизованном состоянии. [11]
Путем аналогичного расчета находим, что молярная теплота адсорбции кислорода на поверхности, содержащей предварительно адсорбированную окись углерода, должна равняться 2 ( 67 - 20 20) 134 ккал / моль, если вся адсорбированная окись углерода превращается в адсорбированный углекислый газ. [12]
Трудно принять также отнесение Блайхолдера и Неффа ( 1962а, б) высокочастотных полос к физически адсорбированной окиси углерода. Адсорбция, по-видимому, специфична по отношению к определенным поверхностям, поскольку покрытие достаточно велико при комнатной температуре, а в некоторых случаях адсорбция является активированным процессом. [13]
Имея это в виду, можно допустить возможность того, что полоса при 2140 см 1 для адсорбированной окиси углерода принадлежит соединениям, связанным с поверхностью только сг-свя-зью за счет неподеленной пары электронов атома углерода. Этим путем можно объяснить существование полос поглощения с частотами 2140 - 2160 см 1, хотя нельзя утверждать определенно, что полосы при частотах, выше 2200 см 1, могут возникнуть в результате образования такой связи. Для получения частот выше 2164 см 1 на поверхности должны быть центры с большей элек-троноакцепторной способностью, чем ВН3, если за эталон элек-троноакцепторной способности атома, с которым координируется окись углерода принять частоту карбонила. [14]
Таким образом, оказывается, что окись алюминия способствует использованию d - электронов платины для образования связи с адсорбированной окисью углерода. Этот вывод трудно примирить с фактом существования на поверхности окиси алюминия сильных кислотных центров Льюиса, которые обсуждались в гл. Можно было ожидать, что электроноакцепторные центры окиси алюминия будут координировать d - электроны металла, препятствуя их участию в адсорбции окиси углерода. [15]
Страницы: 1 2 3 4