Координационное окружение
Cтраница 3
В случае ионов меди достаточно точно развита теория спектров и накоплен экспериментальный материал для многих координационных окружений. Особенности кристаллографической структуры цеолита типа А представляют самостоятельный интерес. [31]
Если при этом расстояния, отвечающие дополнительному координационному взаимодействию, сопоставимы с длинами ковалентных связей и координационное окружение атома олова близко к тригональ-ной бипирамиде или октаэдру для координационных чисел 5 и 6 соответственно, то само наличие такого взаимодействия сомнений кс вызывает. Однако, как будет показано ниже, в ряде случаев координационные взаимодействия оказываются довольно слабыми, и наиболее естественным геометрическим критерием наличия или отсутствия координации между двумя атомами в подобных структурах в принципе должно служить сокращение соответствующего расстояния по сравнению с суммой ван-дер-ваальсовых радиусов. [32]
 |
Строение молекул. а - [ Fe5 ( CO i5C ]. б - Со3 ( СО 9С ( СН3. [ Со3 ( СО 9С ] 2СО. г - ( CH3 4Sn3Fe4 ( CO16. [33] |
СО п другие лппшды, начинай от простых молекул и ионов, где все лнганды образуют обычное координационное окружение атома переходного металла, п кончая такими, где присутствуют более сложные циклические и полиэдрические системы атомов металлов. [34]
Ввиду недостаточной точности спектральных данных при оценке относительных вкладов различных донорных лигандов соответствие сдвига энергии с координационным окружением в настоящее время не может быть проанализировано на количественном уровне. Сравнение соответствующих геометрических свойств металламино-кислотных комплексов в табл. 4 подтверждает, что геометрия координации и конфигурация боковых цепей координированных аминокислот, вероятно, либо различаются очень незначительно, либо совершенно одинаковы. [35]
Структуры оксидов UM6Oi2 представляют собой сравнительно редкие примеры структур, в которых уран ( VI) имеет почти неискаженное координационное окружение в виде октаэдра из шести атомов кислорода ( о структуре 6 - UO3 см. разд. [36]
Структурные типы металлической связи можно подразделить на ряд семейств структурных типов сообразно с преобладающими в каждом семействе координационными окружениями и особенностями связи. Схематически соотношения между этими семействами представлены на рис. 4.31. В порядке увеличения координационного числа среди структур металлических соединений различают следующие семейства структурных типов: 1) тетраэдрические структуры, 2) фазы внедрения, 3) цепные и каркасные фазы, 4) слоистые структуры, 5) фазы типа арсенида никеля, 6) фазы нормальной валентности, 7) электронные соединения, 8) сверхструктуры, 9) фазы переходных металлов, 10) фазы Лавеса. Доля истинно металлической связи, осуществляемой электронным газом в этих соединениях, различна, как и параметры, в которых удобно эту связь описывать. [37]
В некоторых аддуктах XeF2 атом Хе образует две коллинеарные связи, причем один из атомов F входит в координационное окружение атома металла. [38]
Таким образом, по спектрам d - d переходов удается установить три состояния катионов Ш2, отличающихся симметрией координационного окружения кислородом. [39]
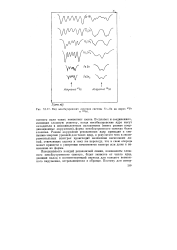 |
Вид мессбауэровских спектров системы Fe-Sn на ядрах 67Fe. [40] |
В сплавах и соединениях, имеющих сложную решетку, когда мессбауэровские ядра могут находиться в неэквивалентных положениях ( иметь разные координационные окружения), форма мессбауэровского спектра более сложная. Разное окружение резонансных ядер приводит к смещению энергии уровней для таких ядер, в результате чего в экспериментальных спектрах происходит наложение нескольких линий, отвечающих одному и тому же переходу, что в свою очередь может привести к уширению компонентов спектра или даже к изменению их формы. [41]
 |
Расщепление энергетических уровней rf - орбиталей в тетраэдри. [42] |
Вследствие сильного экранирования 4 / - орбиталей на состояния, возникающие из различных 4 / - конфигураций, очень мало влияет координационное окружение. [43]
Предположение Вернера о том, чтЬ каждому иону металла свойственно определенное, характерное для него значение координационного числа и тип симметрии координационного окружения, сейчас уже нельзя принять в качестве общего правила. Координационное число вовсе не является неизменной характеристикой атома или иона. Более того, как показывают последние обзоры [1-3], координационное число не является единственным фактором, однозначно определяющим стереохимию соединения. [44]
Различие между ними проявляется в расположении слоев всех производных урана друг относительно друга и в степени участия атомов кислорода слоев в координационном окружении межслоевого катиона. Произведена оценка энергии связи воды в кристаллогидратах урана на различных стадиях дегидратации, определены энтальпии дегидратации. Показано соответствие калориметрических данных с результатами термографических измерений. [45]
Страницы: 1 2 3 4 5