Координационное окружение
Cтраница 4
Происхождение этой фазы можно представить как результат внедрения в кристаллическую решетку МпО атомов кислорода, которые окисляют часть атомов марганца в своем координационном окружении, оттягивая на себя электронную плотность. [46]
Изложенная здесь простая теория позволяет предсказать или, по крайней мере, объяснить найденное экспериментально число неспаренных электронов у ионов переходных металлов в различном координационном окружении. В дальнейшем будет видно, что это удается также и теории валентных связей, хотя для некоторых конфигураций d предсказания этой теории оказываются ошибочными. Большим достоинством теории кристаллического поля ( и теории поля лигандов) является то, что с их помощью можно вычислить также величину магнитного момента. Такие числовые расчеты требуют привлечения довольно сложных методов квантовой механики, например введения спин-орбитального взаимодействия как возмущения первого порядка. Поэтому здесь не будут приведены эти расчеты в общем виде. [47]
 |
Соединения со структурой типа перовскита. [48] |
В структуре перовскита существует такой же октаэдри-ческий каркас, и поэтому октаэдры в этой структуре также могут быть повернуты различными способами с образованием типов координационного окружения атомов А, отличающихся от кубооктаэдра ( координационное число 12) в идеальной кубической структуре. Например, в соединении GdFeO3 [2] КЧ гадолиния понижено до 8 ( слегка искаженная двухшапочная тригональная призма), в то время как в некоторых оксидах АСзВ4О12 ( разд. В этой связи см. также рис. 4.4 0 и описание структуры CoAs3 в разд. [49]
Как и на других алмазоподобных полупроводниках, в роли активных центров выступают преимущественно координационно-ненасыщенные поверхностные атомы и вакансионные дефекты, функциональная способность которых зависит от координационного окружения, особенно в многокомпонентных системах. [50]
Теория поля лигандов в указанном выше смысле рассматривает два вопроса: 1) происхождение и 2) последствия расщепления внутренних орбиталей иона под действием его координационного окружения. [51]
Судя по имеющимся данным, по крайней мере для твердой фазы ограничения геометрического порядка, связа нные с наличием полидентатных лигандов, оказывают также существенное влияние на характер координационного окружения центрального атома. В данном случае выбор координационного полиэдра продиктован в первую очередь размером центрального атома, геометрическими особенностями полидентатного лиганда и его хелатным характером. [52]
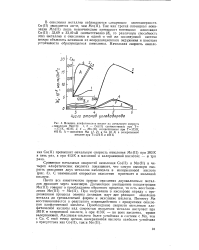 |
Влияние алифатических кислот на начальную скорость. [53] |
Мп ( П) лишь Незначительно превышает потенциал ионизации Со ( II): 33 69 и 33 49зВ соответственно [8], то различную способность этих ( металлов к окислению в одной и той же исследуемой системе можно объяснить влиянием их координационного окружения и констант устойчивости образующегося комплекса. [54]
Ионы ОН - в структурах гидроксосолей связаны с ионами металла, поэтому при небольшом отношении ОН: М координационная группа вокруг металла состоит в основном из атомов кислорода оксо-ионов; при увеличении отношения ОН: М доля ОН - - ионов в координационном окружении металла увеличивается. Этот процесс хорошо иллюстрируется примером гидролиза Zr ( SO4) 2 - 4H2O при 100 С до Zr2 ( OH) 2 ( SO4) 3 - 4H2O и при 200 С до Zr ( OH) 2S04, причем окружение Zr4 рассматривается в сравнении с его окружением в кубическом ZrO2, который является конечным продуктом нагревания этих солей на воздухе. [55]
Тот факт, что координационное число Th4 и U4 по отношению к иону F превышает валентность соответствующих ионов, до известной степени объясняет малую летучесть и трудную растворимость тетрафторидов тория и урана, ибо в кристаллической решетке одни и те же ионы фтора должны входить в состав координационного окружения разных катионов. [56]
Структурная химия теллуратов представляет собой прекрасную иллюстрацию различных способов сочленения координационных октаэдров путем обобщения атомов кислорода с образованием конечных полиядерных групп, цепей или трехмерных сеток. Координационное окружение теллура состоит из 6 кислородных атомов, к части из которых или ко всем присоединен водород. В цепи АХ4 с общими ребрами обобщенными могут оказаться противоположные ( транс) или непараллельные ребра. Существует только одна форма транс-цепи - строго линейная цепь, например, в К [ ТеО3 ( ОН) ], но возможно бесконечно большое число конфигураций цепи с общими непараллельными ребрами ( разд. [57]
На рис. 79 приведена схема строения молекулы. Координационное окружение атома рения составляет четыре атома фосфора и три атома водорода. [58]
Очевидно, что для выявления ключевых стадий вероятного механизма каталитического действия фермента существенно количественное описание металл-лигандного центра как до, так и после связывания субстрата. Поэтому необходимо знать стереохимию координационного окружения иона металла и его ориентацию относительно ближайших аминокислотных остатков, вовлекаемых в связывание субстрата. Кроме того, детальное выяснение химической природы реакционной способности иона металла в ферментах требует установления корреляции между молекулярной структурой, стереохимией, электронной структурой и биологической функцией. Описание принципиального механизма стадий ферментативной реакции на основе сведений о структуре должно соответствовать результатам кинетических исследований, указывающих на сродство к субстратам, вероятную природу промежуточных продуктов реакции и лимитирующие стадии. Предлагаемый механизм должен также находиться в согласии со спектроскопическими данными, которые характеризуют электронные и атомные перегруппировки, включающие фермент и молекулы субстрата. Как и в простых координационных комплексах, детальная информация о строении молекулы позволяет определить электронную структуру и характер связывания ионов металлов и лигандов в белках. Кроме того, характер изменений стереохимии металл-лигандных центров в ходе катализа позволяет понять, какие изменения электронной структуры ответственны за каталитическое действие. Исходя из этого, большое значение для понимания регуляции биологической активности и функции белков приобретает взаимосвязь между молекулярной структурой, стереохимией и электронной структурой центров координации металла. [59]
 |
Кислотные гадроксиды, номинально отвечающие высшим степеням окисления элементов Ш-VIII групп Периодической системы. [60] |
Страницы: 1 2 3 4 5