Оксазола
Cтраница 2
Оксазолы не встречаются в природных веществах; 4Н - оксазо-лоны-5 ( 18), называемые азлактонами, являются промежуточными соединениями в синтезе а-аминокислот. [16]
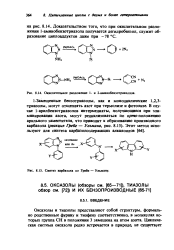 |
Окислительное разложение 1 - и 2-амииобеизотриазолов. [17] |
Оксазолы и тиазолы представляют собой структуры, формально родственные фурану и тиофену соответственно, в молекулах которых группа СН в положении 3 замещена на атом азота. [18]
Нейтральные оксазолы и тиазолы депротонируются сильными основаниями также преимущественно по положению 2; например, тиазол образует магнийорганическое соединение при взаимодействии с этилмагнийбромидом и литируется по положению 2 фенилли-тием при - 60 С. [19]
Соответствующие оксазолы и оксазолины, производимые из се-рина или треонина, встречаются не столь часто. Они представляют группу бактериальных производных железокомплексующих гидр-оксамовых кислот, являющихся факторами роста микобактерий. Нокобактин ( 46) [79] напоминает по структуре микобактин М ( 47) [80] с той, однако, разницей, что вместо оксазолинового кольца первый имеет оксазольное. Структуры гидроксамовых кислот, представляющих собой jV - гидроксилированные производные орнитина, играют важную роль в процессе комплексования железа и присутствуют среди циклических пептидов семейства сидеро-хромных ( см. разд. [20]
Оксазолы менее других азотсодержащих циклов устойчивы к действию кислот и к окислению. Они ароматичны, хотя с этой стороны мало исследованы. [21]
Оксазол - наименее стабильная из циклических систем азолов. Важнейшими его производными являются 5-оксазолоны ( азлактоны), которые можно рассматривать как таутомеры 5-оксиоксазолов. [22]
Оксазол, как такорой, пока еще не был получен. Алкилзамещен-ные оксазолы получаются конденсацией я-галоидкетонов с амидами кислот. [23]
Оксазол, как таковой, пока еще не был получен. Алкилзамещен-ные оксазолы получаются конденсацией а-галоидкетонов с амидами кислот. [24]
Оксазол - наименее стабильная из циклических систем азолов. Важнейшими его производными являются 5-оксазолоны ( азлактоны), которые можно рассматривать как таутомеры 5-оксиоксазолов. [25]
Оксазол смешивают с двумя молями диэтилового эфира малеиновой кислоты, нагревают при 110 С в течение 2 ч и после обработки аддукта соляной кислотой получают диэтиловый эфир 2-метил - 3-окси - 4 5-дикарбоксипиридина с выходом 85 %, температура плавления 140 - 144 С ( лит. Этот диэфир восстанавливают литийалюмогидридом ( LiAlH4) в пиридоксин. Дицианпиридин превращают в пиридоксин гидрогенизацией на палладиевом катализаторе с получением 2-метил - 3-окси - 4 5-диаминометилпиридина ( выход 70 %, температура плавления 290 С, лит. Кондратьевой; однако отсутствие публикаций по технологии метода не позволяет отдать ему предпочтение перед другими методами. [26]
Оксазол и тиазол являются аналогами фурана и тиофена, содержащими вместо атома углерода в положении 3 атом азота. [27]
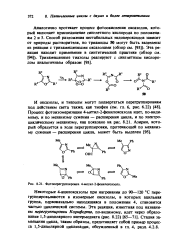 |
Фотоперегруппировка 4-метил - 2-феиилоксаэола. [28] |
И оксазолы, и тиазолы могут подвергаться перегруппировкам под действием света также, как тиофен ( см. гл. [29]
Арилзамещенные оксазола и 1 3 4-оксадиазола различного строения предложены в качестве оптических отбеливателей ( см. гл. Известно применение 2 5-диарилоксазолов в оптических квантовых генераторах ( см. гл. [30]
Страницы: 1 2 3 4