Оксазолона
Cтраница 2
 |
Гидролиз эфирной связи О-аминоацилированных оксикислот и оксиаминокислот водой при 100. [16] |
Окажется ли гидроксил в эфирах оксиаминокислот достаточно реак-ционноспособным, чтобы реагировать также с оксазолонами, будет исследовано в дальнейшем. Во всяком случае эти первые результаты говорят о том, что оксигруппа в белках должна оказаться более активной, чем в свободных оксиаминокислотах. [17]
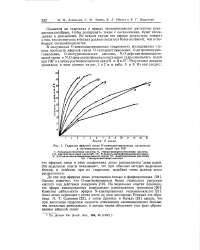
Кинетика образования этилового эфира М - ( М - бензоил а-аминоизобутирил) - ОЬ-аланина из оксазолона и этилового эфира аланина. [18]
Не все аминокислоты, однако, без предварительного ацили-рования способны при действии уксусного ангидрида превращаться в оксазолоны. [19]
Кинетика образования этилового эфира М - ( М - бензоил-а-аминоизобутирил) - 1) Ь - аланина из оксазолона и этилового эфира аланина. [20]
Для проверки своего предположения Мор нагревал х-алкилза-мещенные гиппуровой кислоты9 - 15 с уксусным ангидридом и получил при этом соответствующие оксазолоны. [21]
В опытах с фенилсерином наблюдались аналогичные явления: 2-фенил - 5-оксазолон реагировал в щелочной ацетоновой среде с ацетоном ( III); в растворе бензола оксазолон вообще не вступал в реакцию. [22]
С целью выяснения возможных путей подхода к изучению роли гидроксила в белке мы исследовали реакционную способность гидроксила в оксиаминокислотах, в частности по отношению к оксазолонам; мы ставили при этом и вторую цель - получение эфирной связи аминокислоты по оксигруппе, о чем изложено будет несколько ниже. [23]
При синтезе оксазолонов по методу Бергмана из N-галоидо-ациламинокислоты или из соли N-галоидоациламинокислоты с пиридином, кроме оксазолонов, были получены соединения того же состава, что и оксазолоны, но отличающиеся от последних некоторыми свойствами. [24]
При синтезе высших алифатических а-аминокислот через ок-сазолоны [38] возникают затруднения, вызванные тем, что исходные длинноцеппые альдегиды не всегда доступны и к тому же иногда лишь с плохими выходами образуют оксазолоны реакцией с гиппуровой кислотой. [25]
Оксазолоны 44, обычно называемые азлактонами, представляют собой ангидриды N-ацил аминокислот. [26]
Если атоме азота находится алкильная группа, циклизация [134] может только к полностью нейтральному соединению с цвиттерионной структурой, для которой невозможно написать нейтральную каноническую форму, а только мезоионную. Мезоионные оксазолоны ( названные Хьюзгеном мюнхноны в честь Мюнхенского университета в Германии, где они были открыты) подвергаются быстрому диполярному циклоприсоединению [135] с потерей ССЬ из первоначального аддукта. [27]
В оксазолонах, в молекулах которых R или R представлены оксигруппой, выделить геометрические изомеры не удается. [28]
Способ получения а-аминокислот через оксазолоны ( азлакто-ны) уже давно нашел широкое применение. При гидролизе оксазолоны дают ненасыщенные а-ациламинокислоты, которые затем могут быть прогидрированы до насыщенных ациламлнокислот. [29]
Насыщенные оксазолоны со свободной метиленовой группой в положении 4 чаще всего получают нагреванием N-ацилглици-нов с уксусным ангидридом. Однако не все оксазолоны со свободной метиленовой группой в положении 4 удается получить этим методом. Например, этот метод не пригоден для получения оксазолона из трифторацетилглицина23, а при нагревании фенацетуровой кислоты с уксусным ангидридом19 образуется 2-бензилиден - 3-ацетиламиноксазолидинон - 5 ( VIII), а не 2-бензилоксазолон - 5 ( см. стр. [30]
Страницы: 1 2 3 4