Оксиапатит
Cтраница 2
Поскольку сорбция идет на поверхности кристаллов оксиапатита, такую нестабильность следует отнести к вариациям кристаллической структуры. Это характерно не для кулоновских взаимодействий с их относительным дальнодействием и изотропностью, а, например, для направленных и локальных дипольных взаимодействий. [16]
Из общих рекомендаций, относящихся к хроматографии на оксиапатите как белков, так и НК, отметим предпочтительность использования для очистки биополимеров широких и коротких колонок. Это связано, в частности, с невысокими гидродинамическими характеристиками сорбента. Колонки с оксиапатитом отличаются относительно медленным течением элюента и довольно легко забиваются при измельчении его хрупких кристаллов. С другой стороны, они обнаруживают склонность к образованию каналов для элюента, поэтому иногда имеет смысл осторожно ( чтобы не разрушить кристаллы) перемешивать сорбент, что трудно сделать в узкой и длинной колонке. Верхний слой оксиапатита особенно легко засоряется - его нужно время от времени удалять. Все эти манипуляции облегчаются благодаря тому, что оксиапа-тит не боится контакта с воздухом и даже кратковременного обсыхания колонки. Вместе с тем колонки оксиапатита используют обычно однократно или небольшое число раз ввиду накопления необратимо сорбируемого материала. При расчете необходимого количества сорбента можно исходить из того, что 1 г сухого оксиапатита дает примерно 2 5 мл упакованного объема влажного сорбента в колонке. [17]
В соответствии с различным содержанием двунитевых участков с колонки оксиапатита при постепенном увеличении концентрации фосфатного буфера последовательно элюируются следующие виды НК: однонптевые ДНК и РНК, тРНК, 5S РНК, гибриды РНК-ДНК и двунитевая ДНК. [18]
Ограниченность наших представлений о механизме сорбции кислых белков на оксиапатите с еще большим основанием следует отнести к механизму сорбции основных белков. Вероятно, в ней участвуют кулоновские взаимодействия положительно заряженных остатков аминокислот на поверхности белка с отрицательно заряженными остатками фосфорной кислоты, которые тоже должны быть на поверхности оксиапатита. Об этом говорит более прочная сорбция полилизина и полиаргинина, чем других, более нейтральных полипептидов. Но вполне возможно, что и иные виды взаимодействия здесь играют важную роль. [19]
Полисахариды, в частности гликоген, слабо сорбируются на оксиапатите. [20]
Полисомы, как и двунитевые ДНК, сорбируются на оксиапатите в 0 15 М фосфатном буфере, а элюируются - 0 4 М буфером. Очистку препарата полисом от гликогена удобно вести на стеклянном фильтре, где на влажном бумажном фильтре Whatman № 3 осторожно формируют слой оксиапатита толщиной 2 - 3 мм. [21]
Гофман [76] разделял 1 - и 2-моноглицериды на тонких слоях оксиапатита при 10 С, используя как элюирующий растворитель метилизобутилкетон. В отличие от элюирования на слоях силика-геля при хроматографировании на оксиапатите не удается достаточно четко разделить 1 2 - и 1 3-диглицериды. [22]
Для отделения одного или двух моноглицеридов от белков Хофман [138, 139] использовал оксиапатит, который представляет собой частично гидролизованный фосфат кальция, получаемый щелочным гидролизом однозамещенного основного фосфата кальция. Это более слабый адсорбент, чем кремневая кислота, и на нем можно проводить разделение неионизованных или нейтральных соединений. Эйнакер и Стой [140] готовили оксиапатит следующим образом. Описанную процедуру повторяют три-четыре раза до тех пор, пока рН не перестанет заметно меняться. После этого осадок промывают спиртом, затем ацетоном и высушивают. Сухой продукт просеивают через сито 170 меш. Более грубые частицы можно измельчить на шаровой мельнице и просеять повторно. Эйнакер и Стой [140] сами приготовляли двухосновный фосфат кальция из одноосновного фосфата. [23]
Тремель показали, что в системе трикальцийфосфат-тетракальцийфосфат нет соединения, отвечающего оксиапатиту, но есть эвтектика. Образование же апатитовой структуры при высоких температурах и избытке СаО по сравнению со стехиометрическим соотношением, отвечающим трикальцийфосфату, вызывается воздействием паро в воды. [24]
Фосфатные буферы различных концентраций используются для хро-матографической элюции этих биополимеров с колонок оксиапатита. Замечательно, что нейтральные соли, например NaCl и КС1, в этих случаях не препятствуют сорбции и не годятся в качестве элюентов. Сульфаты, оксалаты и карбонаты также малоэффективны. [25]
Резюмируя, можно сказать, что хроматографическое фракционирование и очистка белков на оксиапатите остаются пока методами эмпирическими, где предсказать результаты и дать заранее определенные рекомендации по выбору оптимальных условий элюции затруднительно. [26]
При этом следует, однако, иметь в виду, что а-фаза ( оксиапатит) является гидроксил апатитом. В реальных условиях, при наличии больших количеств твердой фазы, невозможно исключить влияние водяных паров. Поэтому в действительности обычно существуют не двухкомпонентные системы, а состояния, отражаемые этой частично неверной, диаграммой, с исправлениями, учитывающими, что оксиапатитовая фаза является гидроксилапатитовой фазой, попадающей на плоскость СаО - Р2О5 как проекция части объема трехмерной диаграммы, включающей пары воды. С теоретической точки зрения для знания системы необходимо исследовать такую трехкомпо-нентную систему. [27]
Наличие некоторых примесей или специально добавленных реагентов может существенным образом изменять характер элюции НК с оксиапатита. Например, присутствие ионов ртути и особенно серебра в комплексе с ДНК существенно затрудняет элюцию однонитевой ДНК. [28]
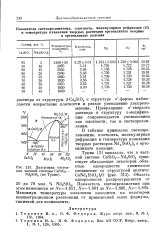 |
Диаграмма состояния частной системы CaSiO3 - Nd2SiO5 ( по Туник. [29] |
Максимум температуры плавления находится на некотором концентрационном расстоянии от приведенной выше формулы, типичной для оксиапатита. [30]
Страницы: 1 2 3 4