Олефипы
Cтраница 2
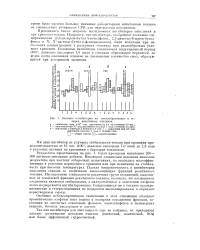 |
Влияние ингибиторов на смолообразование в че. [16] |
Особенно неблагоприятными свойствами в этом отношении обладают ароматические олефипы типа ипдона и полярная смолистая фракция, состоящая из азотистых оснований, фенолов, алкилтиофепов и полимерных веществ, богатых кислородом и азотом. [17]
Особенно ценными в настоящее время для промышленности яшшются низшие олефипы ( С2 - С5) и в первую очередь - этилен и пропилен. [18]
В реакцию Релена можно также с успехом вводить высокомолекулярные гомополимерные олефипы изостроения, такие, как диизобутилен и трипро-пилен и смешанные полимеризаты пропилена с бутиленами. Даже синтетические смазочные масла, получающиеся полимеризацией олефинов под действием хлористого алюминия, присоединяют смесь окиси углерода и водорода в количестве до 50 % от теоретически возможного, определяемого по родановому или йодному числам. При этом они частично подвергаются гидрированию, которому пространственные препятствия почти не мешают. Однако в результате изомеризации двойной связи, происходящей при гидроформилироиании, образуются олефипы, у которых расположение двойной связи благоприятствует реакции Релена. Эти олефипы быстро присоединяют окись углерода и водород, в результате чего равновесно изомеризации смещается в сторону их дальнейшего образования ( см. гл. Асимметричные дила мощенные этилеиы типа H z С СП2, например изобутилеп или 2-мотилбутен - 1, очень легко вступают в реакцию Релепа. [19]
 |
Схема получения адкилсуль-фатов ( типоль сульфированием высокомолекулярных олефинов. [20] |
Линии: I - серная кислота; II - олефипы; III - нейтральное масло; IV - раствор алнилсульфата в поде и спирт; V - циркулирующий пропилр-вый спирт; VI - возврат бензина; VII - нейтральное масло; VIII - паста типоль; IX - проппловый спирт. [21]
Хлоргидрины высокомолекулярных олефинов можно успешно получать действием алкилгипохлоритов на олефипы в водной среде. При этом хлористые алкилы образуются лит г, в незначительной степени. Из органических гипохлоритов для этой цели больше всего подходит щрета-бутилгипохлорит, ( СНЯ) ЯСОС1, получаемый хлорированием тереиг-бутилового спирта при 0 в присутствии раствора щелочи. [22]
В 1875 г. В. В. Марковников, изучавший действие галоидоводородов на олефипы, сформулировал правило, названное его именем. Согласно этому правилу атом галоида всегда присоединяется к атому углерода, наиболее бедному водородом. [23]
Доярепко [61] наблюдали изомеризацию над А120Я производных циклопропана в соответствующие олефипы. С ароматические углеводороды с аллильной боковой цепью изомеризуются в ароматические с пропепильной боковой цепью. В тех же условиях диизобутенил полностью превращается в диизокротил. По мнению Р. Я. Левиной, диаллил над А1203 изомеризуется с большей скоростью, чем над активированным флоридином, хотя Я. М. Слободин [40] и считал изомеризацшншую способность А1203 и флоридина равноценной. [24]
Автор прежде всего стремился описать процессы, в результате которых олефипы образуются в качестве неизбежных продуктов реакции, а затем рассмотреть современные возможности производства олефинов и в первую очередь этилена. Поскольку речь идет преимущественно о пиролитических процессах, в результате которых в определенных условиях протекают реакции ароматизации, то рассмотрены и эти реакции. [25]
В противоположность этому более старый метод превращения карбонильных соединений в олефипы, использующий реакцию Гринья-ра с последующей дегидратацией получающегося карбинола, обычно дает смесь изомерных олефинов. [26]
Весьма пригодны для этой цели низкомолекулярные и высокомолекулярные крекинг-олефины, например тетрамер пропилена ( изододецен), и олефипы, получающиеся при синтезе Фишера-Трошна. [27]
Оксиресвератрол 326 Окситоцин 132 5 - Окситриптамин 258 Л 13 - is - O леанен 210, 211 Олефипы, получение гомологов 152 г ( б - 0лефины, получение 151 Олигосахариды 157, 158 Омматшш 348 и ел. [28]
Первые три представителя ряда олефинов являются при обычных условиях газами, начиная с пептонов С5П) () - жидкостями, а высшие олефипы, начиная с С19П38 - твердыми телами. [29]
В этом случае для присоединения шшдов к карбонильным соединениям требуется несколько минут, в то время как последующее разложение бетаинов на окись фосфина и олефипы часто требует продолжительного стояния при комнатной температуре или нагревания в течение нескольких часов. Следовательно, скорость реакции определяется стадией Б, разложением бетаина. В результате электронодонорпые группы у атома фосфора, несмотря па облегчающее влияние на стадию А, будут затруднять последующее разложение через четырехчленное циклическое промежуточное соединение, поскольку фосфор будет менее склонен к образованию связи с анионом кислорода в бетаине. Так, например, при взаимодействии бензофенона с метилентриметилфосфораном получили лишь бетаин 65, который мог быть охарактеризован в виде иодгидрата 11021, в то время как в случае метилентрифенилфосфорана [ 1 1 в тех же самых условиях получили почти количественный выход олефина. [30]
Страницы: 1 2 3 4