Зависимость - коэффициент - активность
Cтраница 1
Зависимости коэффициентов активности в растворе азот-метан [1] при наиболее высокой температуре ( 122 04 К) близки к обычно наблюдаемым для зеотропных систем с неограниченной растворимостью. Отклонения от идеальности для азота меньше, чем для метана. При наиболее низкой температуре ( 99 82 К) зависимость логарифма коэффициента активности метана от концентрации перестает иметь параболический характер, а при больших концентрациях метана наблюдается характерное отклонение точек от монотонной ( по производной) зависимости. Это отклонение еще можно отнести за счет неточности экспериментальных данных или расчетной процедуры, однако активность метана, по-видимому, превышает единицу. [1]
Зависимость коэффициента активности от различных факторов сложна, и ее определение встречает некоторые трудности. Поэтому в ряде случаев, где не требуется большая точность, в аналитической химии ограничиваются применением закона действия масс в его классической форме. [2]
Зависимость коэффициентов активности 7 - i-от концентрации нитратов уранила ( 1), натрия ( 2) и кальция () в бинарных водных растворах. [3]
Зависимость коэффициента активности от различных факторов сложна и ее определение встречает некоторые трудности, поэтому в ряде случаев, где не требуется большая точность, в аналитической химии ограничиваются применением закона действия масс в его прежней классической форме. [4]
Зависимость коэффициента активности от различных факторов сложна, и ее определение встречает некоторые трудности. Поэтому в ряде случаев, где не требуется большая точность, в аналитической химии ограничиваются применением закона действия масс в его классической форме. [5]
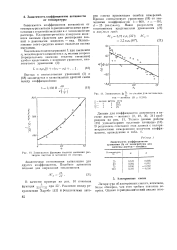 |
Зависимость функции теплоты смешения растворов ацетона и метанола от состава.| Зависимость lg - - от состава для системы аце. [6] |
Зависимость коэффициентов активности от температуры связана термодинамическими уравнениями с теплотой смешения и с теплоемкостью раствора. Калориметрические измерения являются важным средством для расширения знаний о равновесии жидкость - пар. Использование этого средства может оказаться весьма выгодным. [7]
 |
Зависимость коэффициентов активности некоторых сильных электролитов от концентрации их растворов. [8] |
Зависимости коэффициентов активности некоторых сильных электролитов от концентраций их растворов изображены и на рис. 7.2, из которого видно, что в области очень малых концентраций ( меньше 0 01 моль / кг Н20) коэффициенты активности всех электролитов стремятся к единице. С ростом концентрации они уменьшаются и при концентрациях от 0 1 до 1 моль / кг Н2О имеют минимальные значения. В области высоких концентраций коэффициенты активности снова увеличиваются. [9]
Зависимость коэффициента активности от различных факторов сложна и ее определение встречает, некоторые трудности, поэтому в ряде случаев ( в особенности в случае растворов / слабых электролитов), где не требуется большая точность, в аналитической химии ограничиваются применением закона действия, масс в его классической форме. [10]
Зависимость коэффициента активности от различных факторов сложна и ее определение встречает некоторые трудности, поэтому в ряде случаев ( в особенности в случае растворов слабых электролитов), где не требуется большая точность, в аналитической химии ограничиваются применением закона действия масс в его классической форме. [11]
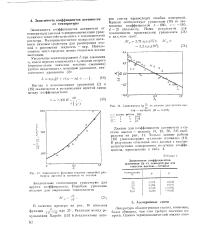 |
Зависиыостъ функции теплоты смешения растворов ацетона и метанола от состава.| Зависимость lg - - от состава для системы ацо. [12] |
Зависимость коэффициентов активности от температуры связана термодинамическими уравнениями с теплотой смешения и с теплоемкостью раствора. Калориметрические измерения являются важным средством для расширения знаний о равновесии жидкость - пар. Использование этого средства может оказаться весьма выгодным. [13]
Зависимость коэффициентов активности электролитов от состава раствора является важной и сложной проблемой физической химии. Для бинарных растворов сильных электролитов существуют удовлетворительные способы описания, основанные на теории Дебая-Хюккеля. Ниже мы попытаемся показать, что обширны экспериментальные данные по смешанным растворам электролитов являются важным полигоном для испытания теорий. [14]
Зависимость коэффициента активности первого компонента от состава имеет вид: In у аХ ЬХ - Давление над чистыми жидкостями равно Р и F2 Найдите константы Генри для обеих жидкостей. [15]
Страницы: 1 2 3 4 5