Зависимость - коэффициент - активность
Cтраница 3
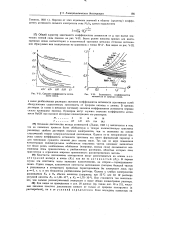 |
Средние коэффициенты активности ионов.| Зависимость коэффициентов активности от природы ионов. [31] |
Общий характер зависимости коэффициентов активности от ц при малых значениях ионной силы показан на рис. V-21. [32]
Характерный ход зависимости коэффициентов активности от состава для систем с различными отклонениями от закона Рауля показан на рис. 1 ( стр. Количественная проверка может производиться по уравнениям ( 70) или ( 184) и заключается в следующем. [33]
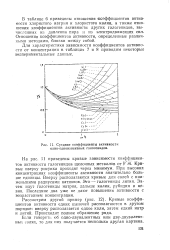 |
Средние коэффициенты активности одно-одновалентных галогенидов. [34] |
Для характеристики зависимости коэффициентов активности от концентрации в таблицах 7 и 8 приводим некоторые экспериментальные данные. [35]
 |
Зависимость Я, Ф и отклонений от идеальности не опре - TSE от концентрации в раство - деляется знаком энтальпии смеше-рах сурьма - кадмии при 500 С м. [36] |
Должна быть известна зависимость коэффициентов активности от температуры, давления и в случае необходимости от других переменных, определяющих состояние. [37]
Параметр, характеризующий зависимость коэффициентов активности от состава, должен определяться по данным о растворимости при постоянной температуре, причем концентрация неконденсирующегося компонента должна быть возможно более высокой, чтобы обеспечить требуемое отклонение от идеальности. [38]
 |
Зависимость Н, Ф и отклонений от идеальности не опре - TS от концентрации в раство - делается знаком энтальпии смеше-рах сурьма - кадмии при 500 С т м. [39] |
Должна быть известна зависимость коэффициентов активности от температуры, давления и в случае необходимости от других переменных, определяющих состояние. [40]
В разбавленных растворах зависимость коэффициента активности от ионной силы раствора для иона, несущего г единиц заряда, описывается предельным законом Дебая-Гюккеля (1.5), выведенным в приближении точечных зарядов. Согласно этому уравнению единственным свойством иона, определяющим значение его коэффициента активности в заданных условиях ( растворитель, ионная сила раствора, температура), является его заряд. [41]
Параметр, характеризующий зависимость коэффициентов активности от состава, должен определяться по данным о растворимости при постоянной температуре, причем концентрация неконденсирующегося компонента должна быть возможно более высокой, чтобы обеспечить требуемое отклонение от идеальности. [42]
В двойных системах зависимость коэффициента активности неэлектролита от состава смеси обычно достаточно хорошо описывается двучленным уравнением Маргул-еса. Уравнение Маргулеса в его простейшей форме распространено Уолом [5] на тройные системы. [43]
Полагая, что зависимость коэффициентов активности компонентов от состава в обеих фазах описывается уравнениями с двумя константами, и подставляя соответствующие значения в ( I. Возможен и обратный расчет. Если константы известны, например из определений у и Y то по уравнениям ( I. [44]
Особенно прост расчет зависимости коэффициентов активности компонентов бинарных смесей от их состава по свойствам азеотропа для систем, в которых образуются регулярные растворы. [45]
Страницы: 1 2 3 4 5