Зависимость - логарифм - коэффициент
Cтраница 2
 |
Зависимость коэффициента Генри для метана от характеристического фактора в двойных жидких растворах. [16] |
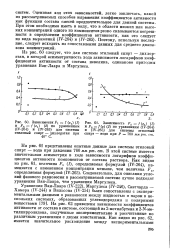
На рис. III.6 показана зависимость логарифма коэффициента Генри k0 ( P02, Т) от характеристического фактора для метана, растворенного в бинарных жидких смесях при температурах 20 и 60 С. Зависимости коэффициента k0 для тройных систем близки к прямым, построенным по данным бинарных смесей метана с индивидуальными углеводородами. [17]
 |
Коэффициент диффузии ионов фосфора как функция 1 / Г.| Схема опыта в электрическом поле. Пунктиром указана мет. [18] |
На рис. 39 изображена зависимость логарифма коэффициента диффузии фосфора 32Р в кристаллах КС1 от обратной температуры. Энергия активации процесса диффузии, найденная лз наклона прямой IgD как функции 1 / Г, составила 3 2 эВ, что является очень большой величиной. Поэтому процесс диффузии атомов радиофосфора можно попытаться представить как явление, обусловленное наличием в кристалле гетерофазных флуктуации. Предположим, что перемещение радиофосфора происходит только тогда, когда он вместе со своим катионным и анионным окружением входит в область, обладающую теплосодержанием жидкого состояния. [19]
На рис. V.6 приведена зависимость логарифма коэффициента диффузии хлористого натрия в сополимерах с различным содержанием исходных мономеров от обратной объемной доли воды в полимерах. [20]
Выражение (3.3) показывает, что зависимость логарифма коэффициента вязкости от обратной температуры должна быть прямолинейной. Это действительно наблюдается для неассоциированных жидкостей типа бензола и тетрахлорида углерода. Для воды зависимость коэффициента вязкости от температуры не описывается приведенным соотношением, что обусловлено частичным разрушением структуры водородных связей с повышением температуры. [21]
На рис, П-13 представлена зависимость логарифма коэффициента активности н-пентана при 25 С от полярности растворителей, выраженной отношением ТкИП / кип - Из графика следует, что при увеличении полярного взаимодействия между молекулами растворителя происходит значительное отклонение поведения растворенного вещества - н-парафина от идеального. [22]
 |
Участки диаграммы состояния. при понижении температурной устойчивости основного компонента при введении примеси ( k 1 ( а и при ее повышении ( k - ( б. [23] |
Важнейший результат, полученный в результате анализа выведенных уравнений, - линейность зависимости логарифма коэффициента распределения от обратной температуры по абсолютной шкале - был экспериментально подтвержден в работах Тармонда, Стразерса [15] и Холла [ 161 для ряда примесей в германии и кремнии. Однако в дальнейшем Трамбором с сотрудниками [17, 18] были обнаружены нарушения этой закономерности, например для примеси олова в германии и кремнии. [24]
 |
Зависимости FI / ( xt ( 1 [ IMAGE ] Зависимость F1 / ( хг ( 1. [25] |
Из рис. 60 следует, что для системы этиловый спирт - дихлорэтан, в которой асимметричность хода зависимости логарифмов коэффициентов активности от состава невелика, одинаково пригодны уравнения Ван-Лаара и Маргулеса. [26]
На рис. 61 представлены опытные данные для системы этиловый спирт - вода при давлении 760 мм рт. ст. В этой системе имеется значительная асимметрия в ходе зависимости логарифмов коэффициентов активности компонентов от состава раствора. Следовательно, для описания условий фазового равновесия в рассматриваемой системе лучше подходят уравнения Ван-Лаара, чем уравнения Маргулеса. [27]
В области частот, где скорость ослабления постоянна и не зависит от числа нулей и полюсов, сдвиг фазы также практически постоянен и составляет 90 на 6 дб на октаву, или я / 2 рад на единицу Y - Общий метод построения диаграмм Боде заключается в использовании лекал, воспроизводящих зависимость логарифма коэффициента усиления и фазы от log / для полюса или нуля на вещественной оси; для комплексной пары нулей или полюсов используется набор подобных лекал. Соответствующим суммированием коэффициентов усиления и фаз для каждого полюса и нуля системы ( смещая частотный срез лекала по оси частот до совпадения радиального расстояния на s - плоскости для каждого полюса или нуля) можно построить результирующий график коэффициента усиления и фазы минимально-фазовой схемы. [28]
При хроматографии на силикагеле часто соблюдается следующее правило: удваивание концентрации полярного компонента в подвижной фазе ведет к уменьшению удерживания в 2 - 2 5 раза. Зависимость логарифма коэффициента емкости от логарифма молярной концентрации полярного компонента обычно линейна. При хроматографии на алкилсиликагелях такая зависимость еще более характерна, однако коэффициенты влияния на емкость для разных сорбатов различны и возрастают с ростом их гидро-фобности. [29]
Выражение ( 17) симметрично относительно замены растворителя и растворенного вещества в области разбавленных растворов. Зависимость логарифма коэффициента активности от концентрации может быть представлена для случая растворов неэлектролитов симметричными кривыми второго порядка. [30]
Страницы: 1 2 3 4