Зависимость - логарифм - коэффициент
Cтраница 3
При хроматографии на силикагеле часто соблюдается следующее правило: удваивание концентрации полярного компонента в подвижной фазе ведет к уменьшению удерживания в 2 - 2 5 раза. Зависимость логарифма коэффициента емкости от логарифма ч молярной концентрации полярного компонента рбычно линейна. При хроматографии на алкилсиликагелях такая зависимость еще более характерна, однако коэффициенты влияния на емкость для разных сорбатов различны и возрастают с ростом их гидро-фобности. [31]
 |
Зависимость коэффициента Генри для метана от характеристического фактора в двойных жидких растворах. [32] |
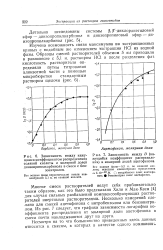
Из табл. III.2 следует, что так же, как и в случае бинарных смесей метана с различными углеводородами, чем ниже значение характеристического фактора, тем выше коэффициент Генри метана. Зависимость логарифма коэффициента Генри от весовой концентрации жидкого раствора для тройных смесей метан-и-гексан-циклогексан, метан-циклогексан-бензол, метан-м-октан-бензол и метан-це-тан-бензол близка к прямой, соединяющей значения логарифмов этих коэффициентов для метана, растворенного в соответствующих индивидуальных компонентах, тогда как эта же зависимость от мольных концентраций отклоняется от прямой, особенно для смесей бензола с высококипящими парафиновыми углеводородами. [33]
Для корреляции данных по равновесию обычно используются интерполяционные уравнения. Интерполяционные уравнения дают зависимость логарифмов коэффициентов активности компонентов от состава в виде уравнения, коэффициенты в котором определяются экспериментально. [34]
Наибольшее распространение для обработки и описания условий равновесия в бинарных системах получили интерполяционные уравнения, составленные с учетом термодинамических требований. Эти уравнения выражают зависимость логарифмов коэффициентов активности компонентов от состава в виде некоторых функций, константы в которых определяются по опытным данным. Уравнения, предложенные разными авторами, различаются видом этих функций и числом фигурирующих в них эмпирических констант. [35]
Если через хроматографическую колонку, в которой в качестве неподвижной фазы нанесен экстрагируемый компонент, пропустить смесь предполагаемых экстрагентов, то легко определить относительные величины изменения потенциальной энер - - гии молекул в экстрагируемом компоненте. Если предположить, что зависимость логарифмов коэффициентов активности от состава имеет симметричный характер, то величины относительных коэффициентов активности экстрагентов в экстрагируемом компоненте будут изменяться симбатно величинам относительных коэффициентов активности экстрагируемого вещества в экстрагентах. Таким образом, минимальному значению относи тельного изменения потенциальной энергии молекул экстр-агента, растворенного в экстрагируемом веществе, соответствует минимальное значение изменения потенциальной энергии молекул экстрагируемого компонента в экстрагенте. [36]
 |
Зависимость lg р от содержания воды в растворителе. 0 5 10 15 20. [37] |
Существуют зависимости селективности от добавок к экстр агенту других веществ. На рис. 2.2 приведена зависимость логарифма коэффициента разделения ( селективности) р от содержания воды в растворителе. Такую высокую селективность может обеспечить применение растворителя с сильной полярностью и малым молекулярным объемом. Однако, чтобы получить надежную оценку свойств растворителя, необходимо выяснить влияние добавок на величину коэффициента распределения К. [38]
 |
Особые виды изотерм обмена. [39] |
Изотермы обмена и кривые титрования не заменяют, а только дополняют друг друга. При изучении сорбции катионов, находящихся в малых количествах, часто определяют сорбцию катиона на фоне высокой и постоянной концентрации кислоты ( gn ж g и сн с) и результаты изображаются в виде зависимости логарифма коэффициента распределения от концентрации кислоты. Последний способ наиболее часто встречается в радиохимических исследованиях. [40]
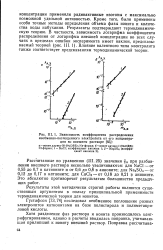 |
Зависимость коэффициента распределения необменно-поглощенного электролита от его концентрации во внешнем растворе. [41] |
Кроме того, были применены особо точные методы определения объема фазы ионита и количества воды набухания. Результаты подтверждают термодинамическую теорию. В частности, зависимость логарифма коэффициента распределения от логарифма внешней концентрации во всех случаях в пределах ошибки эксперимента имеет наклон, предсказываемый теорией ( рис. III. Влияние валентного типа электролита также соответствует предсказаниям термодинамической теории. [42]
Многие смеси растворителей ведут себя приблизительно таким образом, как это было предсказано Хили и Мак-Кеем [4] для случая сильных разбавлений комплексообразующих растворителей инертными растворителями. Несколько измерений сделано для смесей ацетофенона с нитробензолом или бензонитри-лом. Из рис. 7 следует, что графики зависимости логарифма коэффициента распределения от молярной доли ацетофенона в смеси почти накладываются друг на друга. [44]
Зависимости коэффициентов активности в растворе азот-метан [1] при наиболее высокой температуре ( 122 04 К) близки к обычно наблюдаемым для зеотропных систем с неограниченной растворимостью. Отклонения от идеальности для азота меньше, чем для метана. При наиболее низкой температуре ( 99 82 К) зависимость логарифма коэффициента активности метана от концентрации перестает иметь параболический характер, а при больших концентрациях метана наблюдается характерное отклонение точек от монотонной ( по производной) зависимости. Это отклонение еще можно отнести за счет неточности экспериментальных данных или расчетной процедуры, однако активность метана, по-видимому, превышает единицу. [45]
Страницы: 1 2 3 4