Зависимость - скорость - химическая реакция
Cтраница 1
 |
Температурная зависимость констант скорости реакции образования k ( 1 и разложения / с ( 2 йодистого водорода. [1] |
Зависимость скорости химической реакции от температуры является хорошо известным экспериментальным фактом. Обычно скорость реакции растет с повышением температуры. [2]
 |
Температурная зависимость констант скорости реакции образования ( k и разложения ( k йодистого водорода HJ ( по Боден-штейну. [3] |
Зависимость скорости химической реакции хорошо известным экспериментальным фактом, растет с повышением температуры. [4]
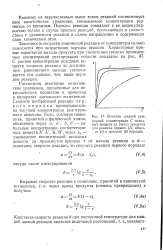 |
Влияние средней суммарной концентрации С исходных веществ на выход продукта для реакции первого ( /, второго ( 2 и третьего ( 3 порядка. [5] |
Зависимость скорости химической реакции от температуры сильно изменяется при возрастании порядка реакции. С ростом концентрации исходных веществ скорость реакции до достижения равновесного выхода увеличивается тем сильнее, чем выше порядок реакции. [6]
Зависимость скорости химической реакции ( или количества превращенного вещества) от условий эксперимента выражается кинетическими уравнениями. Кинетическое уравнение простейшей ( одностадийной) химической реакции может быть составлено на основе системы постулатов. Первым из них является допущение о том, что химические реакции происходят при соударениях статистически независимых частиц. [7]
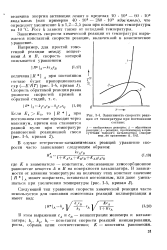 |
Зависимость скорости реакции от температуры при постоянном составе. [8] |
Зависимость скорости химической реакции от температуры выражается константой скорости реакции, включенной в кинетическое уравнение. [9]
 |
Энергия активации прямой и обратной реакции. - - - прямая, - обратная. [10] |
Зависимость скорости химической реакции от температуры устанавливается законом Аррениуса. Сравнение изменения скорости химических реакций при различных температурах может производиться на основании сопоставления коэффициентов скоростей химических реакций, полученных при различных значениях температур. [11]
Зависимость скорости химической реакции от концентрации определяется законом действия масс: скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ. [12]
Зависимость скорости химической реакции от концентрации реагирующих веществ устанавливает закон действующих масс. Частная формулировка этого закона была дана Н. Н. Бекетовым в 1865 г. при изучении влияния давления газообразного водорода на скорость вытеснения им металлов из растворов солей. [13]
Зависимость скорости химической реакции от концентрации реагирующих веществ выражается законом действия масс: скорость химической реакции прямо пропорциональна произведению молярных концентраций реагирующих веществ, взятых в степенях, равных стехио-метрическим коэффициентам соответствующих веществ в уравнении реакции. [14]
Зависимость скорости химической реакции от концентрации реагирующих веществ устанавливает закон действующих масс. Частная формулировка этого закона была дана Н. Н. Бекетовым в 1865 г. при изучении влияния давления газообразного водорода на скорость вытеснения им металлов из растворов солей. [15]
Страницы: 1 2 3 4