Орбиталь - атом - углерод
Cтраница 1
Орбиталь атома углерода свободна. [1]
С какими орбиталями атома углерода они могут перекрываться. [2]
Шесть 2р - орбиталей атомов углерода и шесть их валентных электронов остаются неиспользованными. [4]
 |
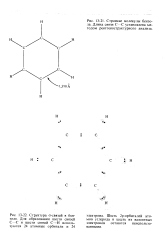
Перекрывание орбиталей этилена и иона Pi3. [5] |
На РЪ - орбиталях атомов углерода в молекуле этилена имеется по одному электрону. На молекулярных орбиталях оба они занимают связывающую молекулярную орбиталь. [6]
 |
Молекула метана.| Молекула этана.| Молекула этена. [7] |
Оси гибридных зр2 - орбиталей атома углерода пересекаются под углом 120, а негибридизованная 2р - орбиталь перпендикулярна плоскости, в которой лежат эти оси. [8]
 |
Энергетическая диаграмма орбиталей охватывает все ато. [9] |
Как показывают расчеты, 2.9 - орбиталь атома углерода по своей энергии резко отличается от ls - орбитали атома водорода. Поэтому по энергетическим условиям комбинация 2в - орбитали атома углерода с четырьмя ls - орбиталями четырех атомов водорода к заметному перекрыванию не приводит, а следовательно, 2в - орбиталь атома углерода в молекуле метана играет роль несвязывающей. [10]
 |
Схемы гибридизованных молекулярных Орбиталей. [11] |
Образование связей при участии sp3 - орбиталей атома углерода особенно характерно для предельных углеводородов и их галогенопроизводных. [12]
 |
Возможная модель молекулы этилена. [13] |
Предположение о том, что определенная гибридная орбиталь атома углерода спаривается с определенной орбиталью атома водорода в случае СН4, оказалось вполне правильным. [14]
Пусть я-связь образуется с участием 2рг - орбиталей атомов углерода. Тогда сг-связи возникают за счет орбиталей 2s, 2px, 2ру каждого атома С. В формировании связей, следовательно, участвуют гибридные р2 - орбитали, оси которых находятся в плоскости Оху. [15]
Страницы: 1 2 3 4 5