Орбиталь - металл
Cтраница 1
Орбиталь металла сферически симметрична и перекрывается с орбиталями всех шести лигандов. [1]
Орбиталь металла имеет области противоположного знака, а потому перекрывается с а-орбиталями лигандов 1 к 3, находящихся на этой же оси по обе стороны от иона металла. [2]
Орбиталь металла сферически симметрична и перекрывается с орбиталями всех шести лигандов. [3]
Орбиталь металла имеет области противоположного знака, а потому перекрывается с а-орбиталями лигандов I к 3, находящихся на этой же оси по обе стороны от иона металла. [4]
Определяют энергию орбиталей металла и комбинации орбиталей лигандов. [5]
Разный тип перекрывания орбиталей металла и лиганда и разный характер симметрии итоговой молекулярной орбитали обусловливают ее так называемый о -, или я -, или 6-характер. Волновая функция я-орбитали при таком повороте меняет знак на противоположный. [6]
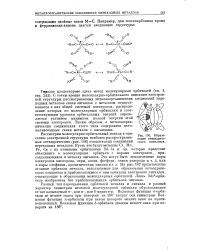 |
Образование октаэдриче-ского комплекса. [7] |
Разный тип перекрывания орбиталей металла и лиганда и разный характер симметрии итоговой молекулярной орбитали обусловливают ее так называемый а -, или я -, или б-характер. Волновая функция о-орби-тали не меняет знака при повороте на 180 вокруг оси симметрии. Волновая функция я-орбитали при таком повороте меняет знак на противоположный. [8]
Орби-лей Ср2 с орбиталями металла тали Fe показаны пунктирными, сходной симметрии. [9]
Рассмотрим на d - орбиталях металла, как же должна меняться энергия d - электронов металлов по мере приближения лигандов к иону металла. Напомним, что d - электроны являются внешними в электронной оболочке иона переходного металла. Но одновременно следует учитывать еще отталкивание между внешними электронами иона металла и отрицательными зарядами на лигандах. Это взаимодействие и называется влиянием кристаллического поля или поля лигандов. В результате него происходит общее повышение энергии d - электронов иона металла, показанное в центральной части рис. 23.22. Правда, не все d - орбитали иона металла реагируют одинаковым образом на влияние поля лигандов. [11]
Одна из заполненных d - орбиталей металла перекрывается с одной пустой d - орбиталью атома фосфора, вследствие чего возникает йя - я-связь. Возможно, что эта связь даже сильнее, чем простая а-связь. Интересно отметить, что такая картина подтверждается тем фактом, что при увеличении электроотрицательности Х - групп, связанных с атомом фосфора, прочность связи металл - лиганд увеличивается. Это может быть предсказано, так как сдвиг электронной плотности к атому фосфора делает его бол ее восприимчивым к электронам, отдаваемым атомом металла. Конечно, усиление а-связи при сближении атомов также должно давать определенный вклад в силу связи. Однако относительная величина этого фактора пока еще не определена. [12]
Одна из заполненных ci - орбиталей металла перекрывается с одной пустой d - орбиталью атома фосфора, вследствие чего возникает 4Я - dn - связъ. Возможно, что эта связь даже сильнее, чем простая т-связь. Интересно отметить, что такая картина подтверждается тем фактом, что при увеличении электроотрицательности Х - групп, связанных с атомом фосфора, прочность связи металл - лиганд увеличивается. Это может быть предсказано, так как сдвиг электронной плотности к атому фосфора делает его бол ее восприимчивым к электронам, отдаваемым атомом металла. Конечно, усиление ст-связи при сближении атомов также должно давать определенный вклад в силу связи. Однако относительная величина этого фактора пока еще не определена. [13]
Одна из заполненных d - орбиталей металла перекрывается с одной пустой d - орбиталью атома фосфора, вследствие чего возникает dn - ил-связь. Возможно, что эта связь даже сильнее, чем простая а-связь. Интересно отметить, что такая картина подтверждается тем фактом, что при увеличении электроотрицательности Х - групп. Это может быть предсказано, так как сдвиг электронной плотности к атому фосфора делает его более восприимчивым к электронам, отдаваемым атомом металла. Конечно, усиление ст-связи при сближении атомов также должно давать определенный вклад в силу связи. Однако относительная величина этого фактора пока еще не определена. [14]
Простейшая попытка разобраться в характере кристаллических орбиталей металла основана на представлении о металле как о совокупности положительных ионов, окруженных весьма подвижной жидкостью, состоящей из делокализованных электронов. Потенциальная энергия электронов в этой жидкости лишь незначительно зависит от их положения. [15]
Страницы: 1 2 3 4
