Орбиталь - металл
Cтраница 3
Теория поля лигандов принимает во внимание взаимодействие орбиталей лигандов с орбиталями металла, по крайней мере в неявной форме. [31]
Далее на схеме показана зона, образованная ( п - 1 -валентными орбиталями металла. Как правило, эта зона узка; степень заполнения ее электронами легко найти из валентной конфигурации атома с учетом формальной степени окисления. В оксиде трехвалентного титана TijOs каждый ион вносит в Sd-зону по одному электрону. [32]
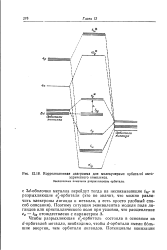 |
Корреляционная диаграмма для молекулярных орбиталей окта. [33] |
Чтобы разрыхляющая е - орбиталь состояла в основном из d - орбиталей металла, необходимо, чтобы d - орбитали имели большие энергии, чем орбитали лигандов. [34]
Ферроцен относится к группе симметрии О5г; в табл. 12 приведены обозначения орбиталей металла и лигандов, взаимодействующих друг с другом, а также трансформационные свойства образующихся из них молекулярных орбиталей. [35]
Во втором случае наблюдается перекрывание заполненной орбитали реагента с вакантной d - орбиталью металла и последующий переход электрона на такую орбиталь. По-видимому, по такому механизму происходит окисление многих ароматических соединений кислородом в присутствии ионов меди ( II), образующих комплекс переноса заряда с ароматическим соединением и окисляющих его до ион радикала. [36]
 |
S Физические свойства аллильных комплексов. [37] |
Эта связь возникает вследствие переходов: а) я-электронов аллильной системы на вакантную орбиталь металла; б) неподеленных пар d - электронов металла на разрыхляющие орбитали я-аллильного аниона с образованием дативных связей. [38]
Результаты расчета, приведенные в табл. 9 - 4, показывают значительную гибридизацию орбиталей металла. [39]
В продукте одноэлектронного восстановления неспаренный электрон может занимать одну из вакантных d - орбиталей металла, так что состояние окисления последнего определится зарядом промежуточной комплексной частицы. [40]
Спектры электронного парамагнитного резонанса позволяют получить, пожалуй, самые непосредственные доказательства перекрывания орбиталей металла и лигандов. Природа электронного парамагнитного резонанса кратко описана в предыдущей главе ( см. стр. При изучении спектров ЭПР было обнаружено, что во многих случаях вместо единственного сигнала, который должна была дать группа d - электронов, локализованных на атоме металла, наблюдается сложная совокупность многих линий, приведенная на рис. 26.22 для ставшего уже классическим случая иона [ IrC. Такую совокупность линий, называемую сверхтонкой структурой, удается удачно объяснить, предположив, что некоторые орбитали иридия и некоторые орбитали координированных с ним ионов хлора перекрываются так, что единственный неспаренный электрон иридия не локализуется на этом ионе, а делокализуется приблизительно по 5 % на каждый ион хлора. [41]
Рис, 27 10, Схема, иллюстрирующая дативное взаимодействие между заполненной - орбиталью металла и свободной Sd-орбиталью фосфора в лигандах типа РХЯ; за ось z принята линия, соединяющая атомы металла и фосфора. Такое же перекрывание с участием 2-орбиталей происходит в плоскости иг. [42]
Очевидно, что при наличии л-лигандов может происходить взаимодействие этих лигандов с заполненными несвязывающими орбиталями металла, с образованием л - МО с более низким энергетическим уровнем, повышением АЕ и стабилизацией а-связи комплекса. [43]
 |
Уровни энергии молекулярных орбиталей в комплексах с КЧ 4 при раз - - 1. [44] |
В заключение следует отметить, что модель углового перекрывания позволяет непосредственно определять энергию перекрывания орбиталей металла и лиганда и оценивать влияние заполнения орбиталей центрального атома на энергию СМО. [45]
Страницы: 1 2 3 4