Зависимость - каталитическая активность
Cтраница 2
В ряде случаев обнаружены зависимость каталитической активности от кислотности активных центров ( рис. 67), подчиняющаяся известному уравнению Бренстеда IgiA lgG - aH0, постепенное снижение ее при дезактивации активных центров основаниями и другие явления, свидетельствующие о количественной связи кислотности и каталитической активности катализатора. При этом оказалось, что для разных реакций оптимальны активные центры бренстедовского или льюисовского типа либо центры, обладающие разной кислотностью. Так, АЬО3 активен при дегидратации спиртов, но не катализирует реакции крекинга. На алюмосиликатах и цеолитах в отношении крекинга или скелетной изомеризации активны центры с высокой кислотностью, в то время как миграция двойных связей и дегидратация происходят на центрах средней и даже слабой кислотности. Это очень важно при выборе оптимального катализатора для того или иного процесса, так как при наличии в нем слишком сильных кислотных центров будут протекать побочные реакции, снижающие его селективность. Такой способ применяют в других типах катализа, когда хотят подавить побочные реакции, протекающие на кислотных центрах поверхности. [17]
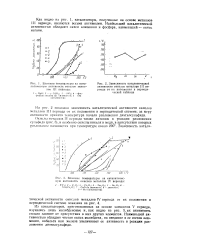
На рис. 2 показана зависимость каталитической активности окислов металлов III периода от их положения в периодической системе; за меру активности принята температура начала разложения диэтилсульфида. [19]
На рис. 1 приведена зависимость каталитической активности Ni / АЬОз в реакциях дегидрогенизации от размера кристаллов Ni. Первоначально [10] это трактовалось как появление оптимума по дисперсности кристаллов в области 70 - 80А, но впоследствии 11 ] оказалось связанным с уменьшением эффективно работающей площади поверхности катализатора. На рис. 1 каталитическая активность рассчитана на единицу веса катализатора. С ростом дисперсности увеличивается удельная поверхность, что должно приводить к возрастанию активности. Однако когда размеры кристаллов становятся меньше 40А, получаются тонкопористые образцы, в которых затруднена диффузия реагентов, а это уменьшает скорость реакции. [20]
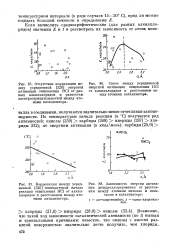
На рис. 45 показана зависимость каталитической активности серебра от концентрации окислов бария, стронция и кальция: для всех добавок эту зависимость можно описать одной кривой с максимумом, лежащим в области концентраций добавки 1 - 3 % ( мольн. [22]
В работе [105] обнаружена зависимость каталитической активности железо-кобальтовых сплавов в реакции разложения аммиака от количества неспаренных d - электронов, приходящихся на атом катализатора. [23]
В работе [105] обнаружена зависимость каталитической активности железо-кобальтовых сплавов в реакции разложения аммиака от количества неспаренных d - электронов, приходящихся на атом катализатора. [24]
В работе [18] показана антибатная зависимость каталитической активности изоэлектронных полупроводников ( Ga2Sea Ga2Tes; GaAs) в реакции разложения гидразина от ширины запрещенной зоны. [25]
Ряд работ посвящен изучению зависимости каталитической активности от молярного соотношения компонентов в каталитической системе литий-алкил-четыреххлористый титан. Фридлендер и Оита [150, 154] сообщили, что при комнатной температуре степень восстановления четыреххлористого титана бутиллитием до трехвалентного состояния зависит как от концентрации реагентов, так и от их соотношения. С увеличением молярного отношения Li / Ti степень восстановления уменьшается. При низких значениях отношения Li / Ti происходит частичное восстановление четырехвалентного титана до трехвалентного. При молярном отношении Li / Ti, равном 4: 1, в продуктах реакции преобладает исходный четырехвалентный титан. [26]
Ряд работ посвящен изучению зависимости каталитической активности от молярного соотношения компонентов в каталитической системе литий-алкил-четыреххлористый титан. Фридлендер и Оита [150, 154] сообщили, что при комнатной температуре степень восстановления четыреххлори-стого титана бутиллитием до трехвалентного состояния зависит как от концентрации реагентов, так и от их соотношения. С увеличением молярного отношения Li / Ti степень восстановления уменьшается. При низких значениях отношения Li / Ti происходит частичное восстановление четы рехвалентного титана до трехвалентного. При молярном отношении Li / Ti, равном 4: 1 5 продуктах реакции преобладает исходный четырехвалентный титан. [27]
Значительный интерес для выяснения зависимости каталитической активности металлов от их электронной структуры представляет изучение сплавов. [28]
Основной интерес для нас представляет зависимость каталитической активности от природы твердого тела. Не менее важно и то, что на поверхности катализатора реакция протекает по другому, более быстрому пути. Как правило, каталитическая активность выше, когда реагенты хорошо адсорбируются на поверхности ( но вместе с тем сохраняют подвижность), а продукты реакции адсорбируются слабо и легко могут удаляться. [29]
Страницы: 1 2 3 4