Зависимость - каталитическая активность
Cтраница 3
Возможно, что такой ход зависимости каталитической активности ( по t) вызван и тривиальными причинами: известно, что окислы с высоко развитой поверхностью значительно легче получить, чем хлориды. [31]
Ниже приведены результаты по изучению зависимости каталитической активности цеолитов разного состава от степени декатионирования или обмена на катионы кальция и лантана. Смешанные формы цеолитов ( кати-он-декатионированные и поликатионные формы) будут рассмотрены в отдельном разделе. [32]
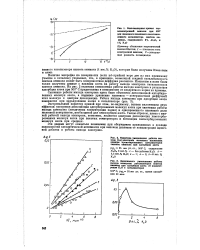
Было показано, что действительно существует зависимость каталитической активности некоторых металлов в реакциях с участием молекулярного водорода от энергии связи фме-н - На рис. 7 представлены вулканообразные кривые, выражающие такую зависимость для реакции гидрирования этиленовых соединений. Общим для этих кривых является то, что на вершинах кривых находится родий, обладающий оптимальной энергией связи Me - Н для гидрирования этиленовых соединений. При гидрировании соединений, содержащих иные типы химических связей, оптимальными оказываются катализаторы с другими значениями QKS-H - Для гидрирования бензола - платина, ацетона - никель и платина. [33]
 |
Линии изоактивности для реакции дегидрирования ызо - С3Н3ОН на окислах ( а и сульфидах ( б металлов. [34] |
На рис. 38, а изображена зависимость каталитической активности окислов в реакции дегидрирования изо - С3Н7ОН от положения металлов в периодической системе. [35]
В последнее десятилетие выполнено много работ, посвященные зависимости каталитической активности от электронно го строения реагирующей молекулы и катализатора. [36]
Многие экспериментальные работы последнего времени посвящены изучению зависимости каталитической активности от степени дисперсности металлических кристаллов. Эти работы были проведены в связи с рассмотрением вопроса о, влиянии строения поверхности кристаллов на активность катализаторов. Однако особенность разбираемой проблемы состоит в том, что далеко не всегда подобные данные действительно позволяют судить о роли структурных эффектов в катализе, так как получаемые экспериментальные результаты, относящиеся к зависимости ( или независимости) удельной каталитической активности от дисперсности, имеют совершенно различный физический смысл, если они соответствуют разным интервалам изменения размеров кристаллов. Это становится ясным, если обратиться к представлениям о строении кристаллов. Ниже приводится краткое изложение общих основ в области применимости этого метода. [37]
 |
Изотерма адсорбции NH3 на свежем SiOa - А12О3 - катализаторе крекинга и на катализаторе, обработанном водяным паром. [38] |
В связи с многочисленными указаниями в литературе о зависимости каталитической активности от поверхностной кислотности или щелочности [75-79], определенной различными методами, были предложены и разработаны также некоторые хроматографические варианты подобных измерений. Дело в том, что высокотемпературные измерения в обычной статической аппаратуре являются достаточно трудной задачей, поэтому в литературе данные об адсорбции молекул с кислыми или основными свойствами немногочисленны. [39]
Топчиевым и Паушкиным [417] было высказано предположение о зависимости каталитической активности соединении трехфтористого бора в реакции полимеризации и электропроводности катализаторов. [40]
Разработка методов измерения поверхности катализаторов позволяет установить характер зависимости каталитической активности от величины поверхности. В этом отношении возможны две категории результатов: 1) каталитическая активность может быть прямо пропорциональна величине поверхности, что должно указывать на однородность поверхности и, следовательно, на правомерность утверждений Бореокова ( см. стр. Это в свою очередь может быть обусловлено двумя причинами: а) наличием на поверхности активных центров, число которых зависит от состава и физического состояния катализатора; б) наличием в катализаторе малых пор, доступных для газов, с помощью которых происходило определение поверхности ( например, для азота по методу БЭТ), и недоступных для больших по размеру молекул органических веществ. [41]
Разработка методов измерения поверхности катализаторов позволяет установить характер зависимости каталитической активности от величины поверхности. В этом отношении возможны две категории результатов: 1) каталитическая активность может быть прямо пропорциональна величине поверхности, что должно указывать на однородность поверхности и, следовательно, на правомерность утверждений Бореакова ( см. стр. Это в свою очередь может быть обусловлено двумя причинами: а) наличием на поверхности активных центров, число которых зависит от состава и физического состояния катализатора; б) наличием в катализаторе малых пор, доступных для газов, с помощью которых происходило определение поверхности ( например, для азота по методу БЭТ), и недоступных для больших по размеру молекул органических веществ. [42]
Эти данные могут оказаться полезными при обсуждении приведенных в докладе зависимостей каталитической активности при высоком давлении от концентрации щелочной добавки и работы выхода электрона. [44]
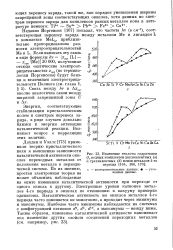 |
Изменение теплоты гидратации Qf водных комплексов двухвалентных ( а и трехвалентных ( б ионов металлов 4-го периода. [45] |
Страницы: 1 2 3 4