Температурная зависимость - скорость - реакция
Cтраница 1
 |
Изменение скорости разложения. [1] |
Температурная зависимость скорости реакции дает энергию активации Е 56 000 кал / моль. [2]
Температурная зависимость скорости реакции подчиняется уравнению Аррениуса для всех взятых растворителей, кроме диоксана. [3]
Температурная зависимость скорости реакции определяется экспоненциальным выражением, известным под названием уравнения Аррепиуса. [4]
Поскольку температурная зависимость скорости реакции представлена показательной функцией, в то время как коэффициент диффузии газов зависит от температуры лишь по степенной функции с показателем менее 2, можно за счет изменения температуры замедлить реакцию с таким расчетом, чтобы она стала лимитировать процесс, или же ускорить реакцию, чтобы определяющим фактором скорости стала диффузия. Переход должен скащваться на зависимости скорости от температуры. [5]
Из температурной зависимости скорости реакции была определена величина Е, которая оказалась равной 14 3 и 15 ккал / молъ для МпСЬ и Со20з соответственно. Подставив это значение в уравнение и используя экспериментальные величины Е, находим Е, равное 15 2 ккал / молъ для МпСЬ и 16 6 ккал / молъ для СогОз. Принимая во внимание, что катализаторы не только зарождают, но и обрывают цепи, величина Е должна быть более низкой, вследствие чего приведенные значения Е несколько завышены. [6]
 |
Влияние температуры при хлорировании. [7] |
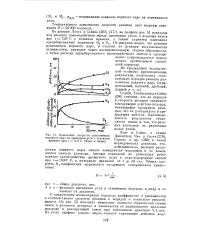
Сравнение температурной зависимости скорости реакций хлорирования этана и хлористого этила, измеренной по количеству прореагировавшего хлора, показало, что температурный коэффициент скорости реакции для этана значительно больше, чем для хлористого этила. Это отчетливо видно из кривых рис. 29, где по оси абсцисс отложены температуры, а по оси ординат - количества израсходованного хлора. [8]
Изучение температурной зависимости скорости реакции иодирования арилмеркурбромидов показало, что изменение скорости в результате введения заместителя обусловлено изменениями как эн-тальпийного, так и энтропийного членов. Известно, что константа р, являющаяся мерой чувствительности реакции к полярному влиянию заместителей, уменьшается при увеличении силы электрофильного агента. [9]
 |
Константы скорости реакции ПБ-ТЭА при 40 С.| Зависимость начальной скорости реакции пере. [10] |
Нами определена температурная зависимость скорости реакции в тех же растворителях в интервале температур от 25 до 65 С. [11]
При изучении температурной зависимости скорости реакций в системе газ - жидкость может встречаться одно усложнение. Когда жидкость ( например, растворитель) достаточно летуча, то при постоянном общем давлении давление ее паров растет с температурой, что ведет к снижению парциального давления газа. [12]
Криволинейные участки температурной зависимости скорости реакции в координатах Арр ниуса свидетельствуют о том, что как при низких, так и при высоких температурах разложение углей не является реакцией первого порядка. [13]
На основе температурной зависимости скоростей реакций ДХДФС и 4 - ( 4 метилфенокси -) - 4 -хлордифенилсульфона с 4-крезолятом натрия1 по значениям экспериментальных констант скоростей реакций графическим решением уравнения Аррениуса определены энергии активации реакций, которые составили 80 8 и 108 3 кДж / моль, соответственно. Из полученных данных следует, что в исследуемом диапазоне температур происходит последовательное замещение атомов хлора в ДХДФС на 4-мстилфенокси-группу, при этом первый атом хлора замещается быстрее, чем второй. Соотношение констант скоростей конкурирующих реакций kijk - 2 увеличивается с понижением температуры, которое, таким образом, способствует селективному замещению одного атома хлора. [14]
Отсюда определяемая из температурной зависимости скорости реакции величина Е будет изменяться с температурой. Рассмотрим выражение энергии активации для реакции, идущей по двустадийной схеме, без лимитирующей стадии, на неоднородной поверхности катализатора. [15]
Страницы: 1 2 3 4 5