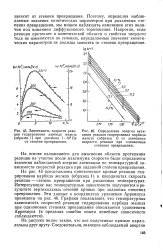
Температурная зависимость - скорость - реакция
Cтраница 4
Определяемая по уравнению Аррениуса энергия активации практически всегда является эффективной величиной и помимо прямого вклада от температурной зависимости скорости реакции содержит вклады от температурных изменений целого ряда параметров системы, прямо или косвенно влияющих на кинетику и термодинамику реакций. [46]
Переход реакции из одной области в другую связан с рядом признаков, наиболее характерным из которых является температурная зависимость скорости реакции. [47]
 |
Изменение потенциальной энергии системы в ходе реакции. [48] |
Для сложных многостадийных процессов температурная зависимость константы скорости может уже не отвечать уравнению Аррениуса, как и температурная зависимость скорости реакции. [49]
Переход реакции из одной области в другую связан с рядом признаков, наиболее характерным из которых является температурная зависимость скорости реакции. [50]
Ранее мы отмечали одну из особенностей газофазного окисления углеводородов - наличие области температур, в которой коэффициент температурной зависимости скорости реакции имеет отрицательное значение. Аналогичный эффект наблюдается к при жидкофазном окислении углеводородов в условиях, когда зарождение цепей происходит преимущественно по гомогенному механизму. [52]
Степень покрытия поверхности катализатора изменяется с температурой, в результате чего температурная зависимость адсорбции, накладываясь на температурную зависимость скорости реакции, будет сказываться на величинах Е, получаемых на опыте. [53]
Структурно-кинетическая модель, заложенная в основу теории химических процессов в замороженных многокомпонентных растворах [3, 19-21], позволяет объяснить экстремальный характер температурной зависимости скорости реакций ( суммарный порядок которых выше первого) в таких системах как конкуренцию противоположно-направленных тенденций, а именно - повышения скорости за счет эффектов криоконцентрирования и уменьшения скорости по мере понижения температуры. Это, в свою очередь, отражается на кинетических особенностях криохимических реакций в замороженных многокомпонентных растворах. НЖМФ существует в довольно широком диапазоне отрицательных температур, в этой микрофазе концентрируются ( при условии достаточной растворимости) компоненты исходного раствора и продукты соответствующих реакций, поэтому такие реакции являются жидкофазными. [54]
Указанное выражение хорошо соответствует экспериментальным данным в широких интервалах изменения температур и поэтому вполне приемлемо как первое приближение к истинной температурной зависимости скорости реакции. [55]
Для реакций с разветвляющимися цепями, развивающимися лавинообразно, условие сохранения равновесия между активированными комплексами и исходными молекулами невыполнимо, температурная зависимость скорости реакции в целом не может быть описана уравнением Аррениуса и понятие теплоты активации для реакции в целом не имеет смысла. [56]
Приводившиеся выше выражения для энергии активации относятся к истинной энергии активации элементарного акта, которая могла бы быть определена из температурной зависимости скорости реакции при постоянной концентрации пар А В, находящихся на нужном для реакции расстоянии. При этом концентрация реакционных пар зависит от температуры как ехр ( - Wi / kT), где Wt - работа сближения реагентов на заданное расстояние. Кроме того, надо учесть, что тепловой эффект элементарного акта Д /, определяющий его энергию активации, отличается от теплового эффекта реакции в целом Д / 0 на величину Wf - Wt, где Wf - работа сближения продуктов реакции. [57]
На основе изложенного для выяснения области протекания реакции на участке после максимума скорости были определены значения наблюдаемой энергии активации по температурной зависимости скоростей реакции при заданной степени превращения. [59]
Страницы: 1 2 3 4 5