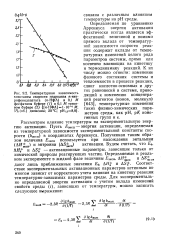
Температурная зависимость - скорость - реакция
Cтраница 3
В табл. 2 приведены результаты изучения температурной зависимости скорости реакции. [31]
Энергия активации может быть вычислена из температурной зависимости скорости реакции и в тех случаях, когда почему-либо не установлен вид кинетического уравнения реакции. Для этого следует пользоваться значениями скорости реакции при различных температурах, вычисленными для одинаковых - степеней превращения исходных веществ. [32]
Энергия активации может быть вычислена из температурной зависимости скорости реакции и в тех случаях, когда почему-либо ие установлен вид кинетического уравнения реакции. Для этого следует пользоваться значениями скорости реакции при различных температурах, вычисленными для одинаковых степеней превращения исходных веществ. [33]
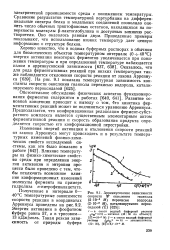 |
Аррениусовские зависимости скорости W окисления гваякола ( 2 - Ю-3 М перекисью водорода ( 2 - 10 - М, катализируемого пероксидазой ( Е. [34] |
Полученные в интервале 0 - 40 С температурные зависимости скорости реакции в координатах Аррениуса приведены на рис. 9.2. Энергия активации в фосфатном буфере равна 57, а в трисовом - 13 кДж / моль. [35]
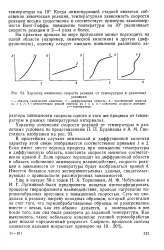 |
Характер изменения скорости реакции от температуры в различных. [36] |
Когда лимитирующей стадией является собственно химическая реакция, температурная зависимость скорости реакции весьма существенна и соответствует примерно закономерности Вант-Гоффа: повышение температуры на 10 увеличивает скорость реакции в 2 - 4 раза и более. [37]
Таким образом, обычно определяемые на опыте из температурной зависимости скорости реакции величины Е являются кажущимися энергиями активации. [38]
Общая энергия активации полимеризации ВП, как следует из температурной зависимости скорости реакции, оказалась равной 24 6 ккал / моль. На основании данных, полученных в опытах по полимеризации ВП на ПАК, испорченной частичной нейтрализацией неполимеризующимся основанием, показано, что в случае слабых полимерных кислот реакция протекает так же в подвижном слое мономера, который окружает макромолекулы ПАК и образует с ними ассоциаты. [39]
Это понятие было введено в химию при изучении природы температурной зависимости скоростей реакций. [40]
Отсюда следует важный вывод, что нет необходимости пользоваться температурной зависимостью скорости реакции в широком интервале температур. Вполне допустимо использование приближенного выражения, правильно описывающего эту зависимость в узком интервале температур. Однако если просто разложить скорость реакции в ряд по степеням разности температур, то потеряется самая характерная особенность явлений горения: способность реакции к экспоненциальному самоускорению. [41]
Критерием того, будет ли волна самоподдерживающейся, яв - ляется температурная зависимость скорости реакции в волне. Сильная зависимость от температуры ведет к нестабильной волне. Для большинства смесей осуществляется этот случай. Все авторы приходят к выводу, что неустойчивость приводит к следующим изменениям в структуре детонационной волны. Зона реакции деформируется и разбивается на ряд возмущений, перемещающихся по поверхности ударного фронта. Предел раздробленности определяется существованием предела времени реакции. Получающаяся структура напоминает структуру спиновой детонации. [42]
Из уравнения Аррениуса следует, что фактор частоты k0 мало влияет на температурную зависимость скорости реакции. [43]
Теория активных столкновений позволяет объяснить порядок би - и мономолекулярных реакций, а также температурную зависимость скорости реакции. Теория позволяет вскрыть физический смысл предъэкспоненциального множителя уравнения Аррениуса, который становится равным числу столкновений молекул в единице объема смеси за единицу времени. [44]
Страницы: 1 2 3 4 5