Основность - анион
Cтраница 1
 |
Ряды последовательности сродства к протону. [1] |
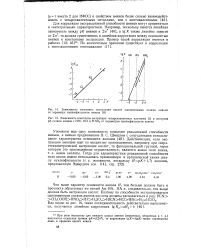
Основность анионов для серии алкокси - и аминосоединений ( табл. 9 - 2) уменьшается с введением метиленовых групп. Этот эффект совершенно противоположен наблюдаемому в растворах, где электронодонорныи характер алкильных групп приводит к возрастанию основности. [2]
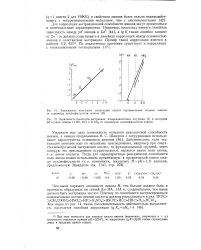
Чем выше параметр основности аниона Я, тем больше должна быть и прочность образуемых им связей Ам-НА... НА и, следовательно, тем выше должна быть экстракция кислот. [4]
Чем выше параметр основности аниона Я, тем больше должна быть и прочность образуемых им связей Ам-HA... HA и, следовательно, тем выше должна быть экстракция кислот. [6]
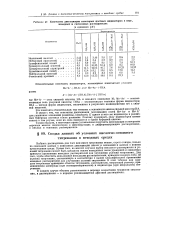 |
Константы диссоциации некоторых цпетных индикаторов в воде, вводных и смешанных растворителях. [7] |
Эта константа относительная; она отнесена к основности аниона сильной кислоты НА. [8]
Переход от протонных к апротонным растворителям резко увеличивает основность анионов из-за отсутствия специфической сольватации. [9]
Сдвиги, индуцированные анионами, грубо коррелируют с основностью анионов, что также можно объяснить влиянием последних на силу водородной, связи. [10]
Поскольку степень переноса протона определяется как основностью растворителя, так и основностью аниона, образующегося при передаче протона растворителю, константа диссоциации тем выше, чем больше основность растворителя и меньше основность аниона. Поэтому сильные неорганические кислоты, основность анионов которых мала, в сильноосновных растворителях диссоциированы в разбавленных растворах практически нацело и, следовательно, в таких растворителях теряется различие в силе таких кислот. По этой причине сильноосновные растворители являются нивелирующими. [11]
В табл. 3 приводится схема, показывающая направление увеличения нуклеофильной реакционной способности и основности анионов. [12]
Поскольку электроны, ответственные за основность [ 3-дикар-бонильного аниона, делокализованы по всей электронной системе соединения, основность аниона остается сравнительно низкой ( ср. R - СН2 - COOR, которые дают продукт конденсации, способный к енолизации. [13]
Альдольные присоединения в общем идут тем быстрее, чем более позитивирован карбонильный атом углерода и чем выше основность аниона псевдооснования. [14]
Если же растворитель слабоосновен, то диссоциация кислот мала и зависит не только от его основности, но к от основности аниона, образующегося при диссоциации кислоты. Основность аниона, в свою очередь, зависит от степени локализации отрицательного заряда на атоме кислорода: чем больше делокализо-ван заряд, тем меньше основность аниона, тем он устойчивее и тем выше константа диссоциации отвечающей ему кислоты. В результате, чем меньше основность растворителя, сем большее значение приобретает стабилизирующее анион влияние заместителей. [15]
Страницы: 1 2 3 4