Пентаммин
Cтраница 1
Пентаммин Чугаева или, отвечающий ему амидотетраммин [ Pt ( NH3) 4NH2Cl ] Cl2 ( синтез см. стр. [1]
Пентаммины [ Pt ( NH3) 3PyNH3Cl ] ( N03) 3 и [ Pt ( NH3Py) 2NH3Cl ] ( N03) 3 и их кислотные свойства. [2]
Пентаммины родия такого осадка не дают, за исключением аквопентамминов, но последние легко перевести нагреванием при 100 - 110 С в соответствующие ацидосоли, которые не будут давать осадка с пирофосфа-том. Чувствительность реакции около 0 2 г.л. Ею пользовался при синтезе Иер генсек для отделения гексамминов от пентамминов. [3]
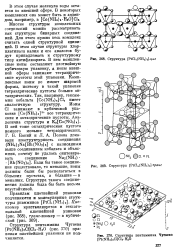 |
Структура [ Р1СЦ ( ГШ3 2 ] - граке. [4] |
Структура пентаммина Чугаева [ Pt ( NH3) 5Cl ] Cl3 - H20 ( рис. 370) правилам плотнейшей упаковки не подчиняется. [5]
Превращение амидотстраммина в пентаммин при действии кислоты или превращение пентаммина в амидотетраммин при добавлении основания вызывает обратимые изменения в ультрафиолетовой области спектра. Гринберг отмечает, что такие соединения можно рассматривать как модель неорганического индикатора. [6]
Спектры гексамминов и пентамминов были совершенно аналогичны, однако эти спектры заметно отличались от спектров как гексанитриловых, так и грыс-этилендиаминовых солей. Кроме того, были обнаружены четыре полосы в спектрах гекса - и пентамми-новых соединений с металлами, отличными от кобальта, и были приписаны аммиачным лигандам. [7]
Для того чтобы получить чистый пентаммин, красные кристаллы растворяют в кипящей воде, смешивают с избытком сероводородной воды. При этом осаждается небольшое количество темно-коричневого осадка сернистого иридия, который отфильтровывают. [8]
Получается, подобно бромиду пентаммина, но вместо бромистоводородной кислоты берут иодистоводородную; соль состоит из светло-желтых блестящих мелких октаэдров. [9]
При этом выяснилось, что вышеупомянутое превращение пентаммина в амидотетраммин сопровождается резким обратимым изменением ультрафиолетового спектра поглощения, так что [ Pt ( NH3) 5Cl ] Cl3 можно рассматривать как модель неорганических индикаторов. [10]
Это отчасти обусловлено тем, что фотохимия пентамминов кобальта и хрома, ближайших электронных аналогов родия, уже достаточно детально изучена. Возбуждение Rh ( NH3) 5Cl2 в области первой полосы поля лигандов ( ППЛ) приводит к полной аквотации хлорида. В рамках классических правил Адамсона [15] трудно объяснить приведенные здесь результаты. [11]
Очень легко подобным же образом изображать строение также пентамминов и тетрамминов. [12]
Превращение амидотстраммина в пентаммин при действии кислоты или превращение пентаммина в амидотетраммин при добавлении основания вызывает обратимые изменения в ультрафиолетовой области спектра. Гринберг отмечает, что такие соединения можно рассматривать как модель неорганического индикатора. [13]
Очень легко подобным же образом изображать - строение также пентамминов и тетрамминов. [14]
Светло-желтый осадок в основном состоит из непрореагировавшего триаммина с примесью пентаммина. Весь цис-тетраммин находится в растворе. [15]
Страницы: 1 2 3 4