Пентацен
Cтраница 4
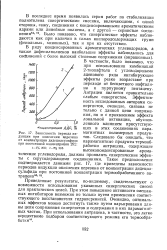 |
Зависимость периода индукции при окислении церезина от концентрации дидецилсульфида при постоянной концентрации 252. [46] |
В частности, было показано, что при использовании комбинаций 2-тконафтола с углеводородами аценового ряда ингибирующие эффекты резко возрастают при переходе от бесцветного нафталина к пурпурному пентацену. Антрацен является сравнительно слабым синергистом. Эффективность исследованных авторами синергистов, очевидно, связана не только с длиной цепи сопряжения, но и с проявлением эффекта локальной активации, обусловленного влиянием присутствующих в этих соединениях парамагнитных полимерных продуктов. [47]
Пентален 469 Пентаметилбензол 27 Пентаметилендиамин 299, 302 Пентантрикарбоновая кислота 584, 623 Пентафенилмышьяк 404 Пентаоенилсурьма 406 Пентаоенилфосфор 404 Пентаоторанилин 49 Пентафторбромбепзол 49 Пентаотортолуол 51 Пентаоторфенол 49 Пентафторхлорбензол 49 Пентахлортолуол 51 Пентацен 239 Пентенилпенициллин 295 Пентозы, дегидратация 259 Пепсин 653, 700, 701 Пепсиноген 701 Пептидазы 653 Пептидсинтетазы 713 Пептиды, синтез 664 ел. [48]
Сравнение азулена и пентацена, которые оба окрашены в синий цвет, часто упоминается как указание на особый электронный, механизм, ответственный за синий цвет азулена, так как последний имеет всего пять формальных двойных связей по сравнению с девятью такими связями пентацена. Однако это сравнение не имеет смысла, так как синий цвет обоих углеводородов вызван переходами различных типов. Полоса азулена, соответствующая длинноволному переходу пентацена, это полоса, лежащая в области 400 мц. [49]
Ацены образуют с кислородом внутренние перекиси ( фотоокиси) тем легче, чем большее число ядер они содержат. Пентацен и гексацен взаимодействуют с кислородом воздуха почти так же легко, как свободные радикалы. По этой причине ранее считали, что ацены представляют собой свободные дирадикалы; однако впоследствии в результате измерения магнитной восприимчивости было доказано, что эти соединения диамагнитны. Взаимодействие с кислородом осуществляется через три-плетное состояние ( см. выше), однако энергия возбуждения у высших аценов гораздо меньше, чем у антрацена; таким образом, реакция наблюдается ( у пентацена) даже в отсутствие света или при слабом освещении. [50]
Ацены образуют с кислородом внутренние перекиси ( фотоокиси) тем легче, чем большее число ядер они содержат. Пентацен и гексацен взаимодействуют с кислородом воздуха почти так же легко, как свободные радикалы. По этой причине ранее считали, что ацены представляют собой свободные дирадикалы; однако впоследствии в результате измерения магнитной восприимчивости было доказано, что эти соединения диамагнитны. Взаимодействие с кислородом осуществляется через три-плетное состояние ( см. выше), однако ( энергия возбуждения у высших аценов гораздо меньше, чем у антрацена; таким образом, реакция наблюдается ( у пентацена) даже в отсутствие света или при слабом освещении. [51]
Тетрацен и пентацен выделяются среди других аренов своеобразными физическими свойствами. Тетрацен образует желто-оранжевые кристаллы с температурой плавления 357 С, а пентацен - сине-фиолетовые кристаллы с температурой разложения более 300 С. При пониженном давлении тетрацен и пентацен возгоняются. [52]
Пентацен, шш2 3 6 7-дибензантрацен, ( XIII) довольно легко реагирует с малеиновым ангидридом ( кипячение в ксилоле в течение 10 мин. Совершенно аналогично был получен аддукт пентацена и с п-бензо-хиноном. [53]
Пентацен, нли2 3 6 7-дибензантрацен, ( XIII) довольно легко реагирует с малеиновым ангидридом ( кипячение в ксилоле в течение 10 мин. Совершенно аналогично был получен аддукт пентацена и с л-бензо-хиноном. [54]
Страницы: 1 2 3 4