Перекрывание - р-орбиталь
Cтраница 1
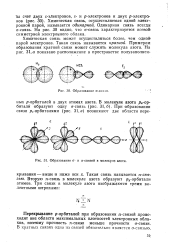 |
Образование а-связи.| Образование а - и я-связей в молекуле, азэда. [1] |
Перекрывание р-орбиталей при образовании л-связей происходит вне области максимальных плотностей электронных облаков, поэтому прочность л-овяэи меньше прочности а-связи. [2]
Такое дополнительное перекрывание р-орбиталей атомов С-2 и С-3 сопровождается выигрышем энергии. Теплота гидрирования диенов с несопряженными кратными связями, например пенгадиена-1 4, составляет 250 кДж / моль. [3]
Такое дополнительное перекрывание р-орбиталей атомов С-2 и С-3 сопровождается выигрышем энергии. Теплота гидрирования диенов с несопряженными кратными связями, например пентадиена-1 4, составляет 250 кДж / моль, а для бутадиена она равна 240 кДж / моль. [4]
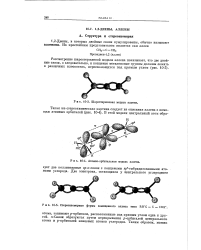 |
Шаростержневая модель аллена.| Стереоизомерные формы замещенного аллена типа RR C С CRR. [5] |
Связи образуются путем перекрывания р-орбиталей центрального атома и р-орбиталей концевых атомов углеродов. [6]
Так как для эффективного перекрывания р-орбиталей они должны быть параллельны, исходные С - Н - и С - - Х - связи, очевидно, также должны быть параллельны, если стадии 1 - 4 сливаются в одностадийный процесс. Должны ли они быть транс - или цис - относительно друг друга, из этих соображений установить нельзя, хотя аналогия с SN2 реакцией приводит к предпочтительности траке-ориентации. [7]
Так как для эффективного перекрывания р-орбиталей они должны быть параллельны, исходные С - Н - и С - Х - связи, очевидно, также должны быть параллельны, если стадии 1 - 4 сливаются в одностадийный процесс. Должны ли они быть транс - или цис - относительно друг друга, из этих соображений установить нельзя, хотя аналогия с S - реакцией приводит к предпочтительности траис-ориентации. [8]
Двойной связи углерод-углерод соответствует перекрывание р-орбиталей, занятых неиспользованными третьими 2 -электро-нами. Рисунок показывает, почему вокруг двойной связи затруднено вращение: чтобы один из атомов углерода вращался вокруг оси, соединяющей центры двух атомов углерода, необходимо нарушить перекрывание л-орбиталей. [9]
В приведенном выше изображении перекрывание заштрихованных р-орбиталей приводит к образованию новой двойной связи в продукте реакции. Двойная связь, нарисованная как СС, присутствует и в исходном диенофиле, и в продукте реакции. [10]
Эти связи образуются вследствие перекрывания р-орбиталей атома кислорода с d - орбиталями атома серы. В результате этого атом кислорода, сохраняя свою полярность, становится менее основным, чем можно было бы ожидать, так как ослабляется р-характер неподеленной пары электронов атома кислорода. Эта связь отличается также от карбонильной связи и в том отношении, что какие-либо группы с двойными связями при присоединении к атому серы не лежат в плоскости SO, и эффекты сопряжения поэтому сильно ослаблены. Частоты колебаний SO при различном химическом окружении достаточно характеристичны. Значения этих частот приведены в табл. 6.1. Новые данные были получены главным образом в процессе исследования основности или структурных исследований циклических систем, поэтому они не полные. В этой главе в первую очередь обсуждаются новые данные, а затем следуют разделы, посвященные отдельным факторам, определяющим точное значение частоты SO в различных конкретных случаях, и разделы, посвященные донорным свойствам этой связи, проявляющимся в эффектах растворения. [11]
Так как в этом случае перекрывание р-орбиталей меньше, чем при образовании а-связей, то полосы поглощения л - - п - переходов занимают, как правило, промежуточное положение между полосами а-о - и M - - JI - переходов. [12]
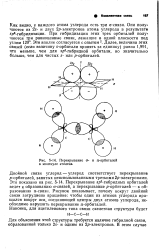 |
Перекрывание а - и я-орбиталей в молекуле этилена. [13] |
Двойной связи углерод - углерод соответствует перекрывание р-орбиталей, занятых неиспользованными третьими 2р - электронами. Рисунок показывает, почему вокруг двойной связи затруднено вращение: чтобы один из атомов углерода вращался вокруг оси, соединяющей центры двух атомов углерода, необходимо нарушить перекрывание я-орбиталей. [14]
Согласно качественным представлениям теории молекулярных орбиталей, перекрывание р-орбиталей атомов углерода и кислорода с образованием л-связи приводит к появлению 1) связывающей ( л) молекулярной орбитали, которая близка по энергии атомной орбитали кислорода и в которой существует несимметричное распределение заряда между двумя атомами в пользу атома кислорода, и 2) разрыхляющей ( я) орбитали с более высокой энергией, которая близка по энергии атомной орбитали углерода. Существует множество теоретических работ, посвященных карбонильной группе, и ст, я-модель углерод-кислородной двойной связи не является единственным употребимым подходом. [15]
Страницы: 1 2 3 4