Перенос - электронная плотность
Cтраница 1
 |
ВЗМО и НСМО перекиси водорода, точечная группа С2 [ энергии взяты из работы Fink W. Н., Allen L. С., J. Chem. Phys., 46, 2261 ( 1967 ]. [1] |
Перенос электронной плотности на орбиталь электрофила совершается в небольшой степени. [2]
Перенос электронной плотности с атома N на связь 81 - К обусловливает высокий электронодонорный эффект силатранильной группы, высокий дипольный момент [ ( 16 9 - 23 3) - 10 - 30 Кл - м ], а также легкую поляризуемость связи 81 - К. [3]
Таким образом, необходим перенос электронной плотности от лиганда к металлу, чтобы стабилизировать металлы в высокой степени окисления. Также необходимо, чтобы лиганд обладал достаточной электроотрицательностью. [4]
 |
Строение трикарбонил ( циклогеп-татриен молибдена. [5] |
Возможно, в результате переноса электронной плотности от колец к металлу ареновые комплексы более чувствительны к окислению. Даже [ Сг ( СбНбЬ ] ( хотя Ее - 36) окисляется до катиона [ Сг ( С6Н6) 2 ] на воздухе. [6]
Вероятно, при координации происходит перенос электронной плотности с металла на молекулу непредельного соединения. Не исключено, что в случае ацетиленовых и диеновых углеводородов этот процесс завершается окислительным присоединением Un к активному центру. [7]
На какую АО Pd происходит перенос электронной плотности с нуклеофилом. [8]
Резонансная константа ай служит мерой переноса электронной плотности по механизму сопряжения. [9]
Уменьшение прочности связи обусловливается большим или меньшим переносом электронной плотности со связи центральный ион - лиганд на одну из низкоэнергетических связевых электронных орбиталей внешнесферного катиона. [10]
С одной стороны, вследствие сверхсопряжения и переноса электронной плотности НЭП на другие орбитали увеличивается порядок связи О-О и уменьшается НЭП-НЭП-отталкивание, что отражается в укорочении связи О-О. С другой стороны, эффективное л - а ( С-0) - взаимодействие увеличивает заселенность разрыхляющей орбитали и дестабилизирует связь С-О, что вызывает ее удлинение. Действительно, из рис. 2.27 видно, что в области Ф - 90 наблюдается увеличение г ( С-О) примерно на 0.01 - 0.02 А. [11]
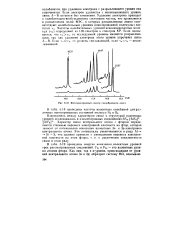 |
Фотоэлектронный спектр газообразного азота. [12] |
Характер связи центрального атома с фтором определяется степенью переноса электронной плотности на фтор, которая зависит от потенциалов ионизации валентных 3s - и Зр-электронов центрального атома. [13]
Некоторое понижение кратности этой связи можно объяснить также уменьшением переноса электронной плотности с кислорода на Sd-орбитали серы вследствие конкуренции за заселение данных орбиталей с nd - орбиталей металла. Таким образом, проведенное качественное рассмотрение, а также результаты полуэмпирических квантово-химических расчетов указывают на некоторое рслабление связи S - О при координации ДМСО через серу. Увеличение же частоты валентного колебания в этом случае следует, по-видимому, связывать не с усилением указанной связи, а с усложнением силового поля, действующего на атом кислорода в частности за счет электростатического взаимодействия металл - кислород. [14]
Привнесение извне электронной плотности - восстановление ГПС - делает более вероятным перенос электронной плотности с атома кислорода на металл. Молярный коэффициент поглощения при этом увеличивается почти на порядок. [15]
Страницы: 1 2 3 4