Перенос - электронная плотность
Cтраница 3
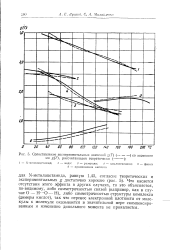 |
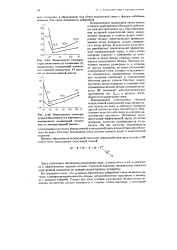
Сопоставление экспериментальных значений g ( T ( - - - - - - - - - - со значениями g ( T, рассчитанными теоретически ( - - - - - - - -. [31] |
Что касается отсутствия этого эффекта в других случаях, то это объясняется, по-видимому, либо симметричностью связей ( например, как в случае О - Н О - Н), либо симметричностью структуры комплекса ( димеры кислот), так что перенос электронной плотности от молекулы к молекуле оказывается в значительной мере скомпенсированным и изменение дипольного момента не проявляется. [32]
Второй способ, предложенный нами для увеличения эффективного заряда иона-катализатора - это использование в качестве активаторов лигандов, образующих с ионом металла обратные я-дативные связи. Перенос электронной плотности по я ( М - - Ь) - связи от металла к активатору также приводит к увеличению положительного заряда центрального иона, а следовательно, и его каталитической активности. [33]
Большую информацию о строении карбонильных комплексных соединений дает ИК спектроскопия, так как частота валентного колебания карбонильной группы весьма чувствительна к изменениям заселенности ее я-молекулярных орбиталей. Перенос электронной плотности с металла на разрыхляющие я-орбитал и оксида углерода ( II) вызывает уменьшение кратности связи, силовой постоянной и частоты колебания связи С - О. [34]
Здесь пунктиром обозначена водородная связь, а знаки и 5 - относятся к эффективным зарядам атомов. Стрелкой показано направление переноса электронной плотности по донорно-акцепторному механизму. [36]
Один из них состоит в замене воды во внутренней координационной сфере катализатора на координирующийся органический растворитель с меньшей основностью, чем у воды. Вследствие более слабых донорных свойств активатора перенос электронной плотности от его молекул к металлу меньше, чем от молекул воды и это приводит к увеличению эффективного заряда катализатора. Однако по этой же причине прочность комплексов металла с такими активаторами будет меньше прочности акво-комплексов, и для вытеснения воды из координационной сферы металла необходимо использовать большие концентрации активатора. В качестве таких активаторов были изучены диоксан, этанол, глицерин и масляная кислота, которые хорошо смешиваются с водой. [37]
Взаимодействие ионов металлов с макроциклическими лигандами определяется как электростатическими силами, так и образованием ковалентной связи. Первый тип взаимодействия не связан с переносом электронной плотности с иона металла на донорные атомы и в обратном направлении. При этом происходят притяжение разноименных электрических зарядов, ион-дипольное взаимодействие или поляризационное взаимодействие, ион-поляризованная связь. [38]
Поляризация ( см. рис. 5, в) приводит к переносу электронов внутри каждой из молекул: от протона Н - мостика к остальной части молекулы донора протона и от атомов Н группы СН2 к атому О формальдегида. Перераспределение электронов между молекулами выражается в некотором переносе электронной плотности от молекулы акцептора протона к донору протона. [39]
Поляризация ( см. рис. 5, в) приводит к переносу электронов внутри каждой из молекул: от протона Н - мостика к остальной части молекулы донора протона и от атомов Н группы СНг к атому О формальдегида. Перераспределение электронов между молекулами выражается в некотором переносе электронной плотности от молекулы акцептора протона к донору протона. [40]
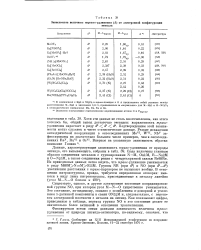 |
Зависимость величины транс-удлинения ( А от электронной конфигурации. [41] |
Существует, однако, и другое электронное состояние координированной группы N0, при котором угол М - N-О существенно уменьшается. Это состояние, по-видимому, связано с ослаблением я-донорной и усилением я-дативной компоненты в связи ON M и, следовательно, с переносом электронной плотности с металла на лиганд. Как показывают цифры, приведенные в таблице, переход группы N0 в это состояние делает ее значительно более активной в отношении трансвлияния. [42]
Наличие минимума на рис. 2.27 свидетельствует о том, что при практически ортогональном расположении заместителей у пероксидной связи происходит ее стабилизация. Поскольку низкая прочность связи - О-О определяется отталкиванием НЭП атомов кислорода, укорочение связи СНО указывает на то, что НЭП вовлекаются во взаимодействия с другими орбиталями пероксидной молекулы с переносом электронной плотности на соседние связи и атомы. Это уменьшает заселенность несвязывающих орбиталей атомов кислорода и, следовательно, снижает НЭП-НЭП-отталкивание, стабилизируя скошенную структуру пероксида. [43]
В настоящее время водородная связь описывается, всходя из до-ворно-анцепторной модели. Особенностью н-связи является и обстоятельство, что при этом взаимодействии используется вакантные орби - али атома водорода группы А - н так что протон в системе А - Н - - В играет роль посредника при переносе электронной плотности от атома В к атому А. [44]
В кристаллах окислов обычно часть отрицательного заряда иона Оа - переходит на катион и таким образом, хотя ступень востановления [3] кислорода остается формально неизменной, равной двум, степень ( или окислительно-восстановительное состояние, как это принято в мировой литературе) в окислах различных металов может быть самой разнообразной. Начиная с [ ВеО ] или [ В2О3 ], где доля ковалентности в связях велика, а заряды ионов малы, переходим к таким веществам, как [ ВаО ] или [ ZnO ], в которых перенос электронной плотности от двухзарядного аниона к катиону сравнительно невелик. [45]
Страницы: 1 2 3 4