Персульфат-ион
Cтраница 1
Персульфат-ион в водных растворах является очень сильным окислителем ( Е - 2 1 В) и широко применяется в аналитических целях. Реакции этого окислителя интересны сами по себе, их механизм подробно рассмотрен в обзоре Уилмарта и Хейма [ 1331, в котором особый интерес представляет обсуждение каталитических и цепных реакций персульфата. По всем этим вопросам читатель может обратиться к указанному обзору. [1]
Персульфат-ион на холоду окисляет только железо, но не ванадий; четырехвалентный ванадий затем медленно титруют раствором марганце-вокислого калия. [2]
Персульфат-ион на холоду окисляет только железо, но не ванадий; четырехвалентный ванадий затем медленно титруют раствором марганцево-кислого калия. [3]
При оттитровывании персульфат-ионов солью железа к анализируемому раствору прибавляют в избытке титрованный раствор соли железа ( П) и соль серебра, каталитически ускоряющую реакцию восстановления персульфата. Определению мешают органические вещества, так как реакция между персульфат-ионами и Fe ( II) индуцирует окисление органических веществ. Бромиды подавляют такие индуцированные реакции окиеления. Разработан [1003] метод определения персульфат-ионов в присутствии этанола, метанола, аллилацетата, аллилового спирта и метил-изопропиенилкетона с применением бромида натрия в качестве ингибитора индуцированных реакций. [4]
Такими окислителями являются персульфат-ион - Ь2О и пермаиганат-ион MnOj. [5]
Как показано Крюковой1, персульфат-ион S2Os - дает волну восстановления на ртутном капельном электроде при 0 3 в ( нас. [6]
 |
Структура молекулы пероксида водорода. [7] |
Перегонка кислого раствора, содержащего персульфат-ион, приводит к его разложению с образованием Н2О2 и сульфат-иона. [8]
Перекись водорода получают электролитическим образованием персульфат-иона и последующим его гидролизом. [9]
Опыты ведут так, что персульфат-ионов в смеси много больше, чем тиосульфат-ионов. [10]
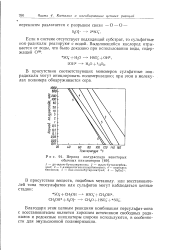 |
Период полураспада некоторых обычных инициаторов. [11] |
Благодаря этим цепным реакциям комбинация персульфат-иона с восстановителем является хорошим источником свободных радикалов и редоксные инициаторы широко используются, в особенности для эмульсионной полимеризации. [12]
Альтернатииный механизм [9] предусматривает атаку персульфат-иона па фенолят-анион по атому кислорода, а не углерода. [13]
При окислении n - фенетидина персульфат-ионом образуются окрашенные продукты реакции. [14]
В нейтральных растворах или в слабых растворах уксусной кислоты персульфат-ион окисляет бензидин до бензидиновой сини. [15]
Страницы: 1 2 3 4