Персульфат-ион
Cтраница 2
Аналогичное явление наблюдается при окислении As ( IlI) персульфат-ионом. [16]
Проверка неравенства (1.66) была осуществлена на примере реакции между персульфат-ионом и иодил-ионом в водном этаноле, а также на примере реакции между ионами те-трабромфенолсульфофталеина и гидроксила в водных смесях метанола и этанола. Проверка неравенства (1.67) была осуществлена на примере реакции между ионом аммония и цианат-ионом в водных смесях метанола и этиленгликоля. Во всех случаях было найдено, что теория соответствует наблюдаемым результатам. [17]
Вследствие экспериментальных трудностей первый из этих процессов ( окисление сульфат-иона в персульфат-ион) не подвергался такому же тщательному исследованию, как остальные, но есть основания полагать, что катализаторы для разложения перекиси водорода и в этом случае снижают выход по току. Так как надсерная кислота может быть получена действием концентрированной перекиси водорода на серную кислоту, а персульфат получается при окислении сульфата фтором, то весьма возможно, что агентом анодного окисления являются либо перекись водорода, либо радикалы гидроксила. [18]
Такой спад тока был обнаружен Крюковой ( 1949) при электровосстановлении персульфат-ионов. [19]
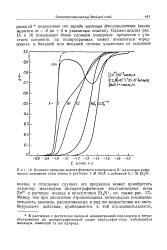 |
Влияние природы аниона фонового электролита Х - на полярографическое поведение иона цинка в растворе 1 М NaX с добавкой 0 1 М Et4N. [20] |
В растворах с достаточно высокой концентрацией перхлората и тетра-этиламмония на полярографической волне персульфат-иона наблюдается минимум, имеющий ту же природу. [21]
Ничтожные количества серебра оказывают резко выраженное активирующее действие на реакцию окисления п-фенетиди на персульфат-ионом, катализируемую соединениями марганца и. Возможно, что основной причиной такого действия является образование комплексных соединений при реакции между катализатором и активатором, которые имеют исключительно высокую каталитическую активность. [22]
Для определения содержания серебра в растворе методом фиксированной концентрации использовали реакцию окисления л-фенитидина персульфат-ионами, в которой соединения Мп ( II) являются катализатором, а соединения серебра - активатором. [23]
Для реакций между двух - и одновалентным ионами электростатические эффекты больше, нежели для реакций между одновалентными ионами; это значит, что отношение неэлектростатического потенциала к электростатическому меньше для реакции между персульфат-ионом и иодид-ионом, нежели для реакции иона аммония с цианат-ионом. Для первой реакции в случае водных смесей этанола соответствующее отношение оказывается равным 3 8; для реакции между двухвалентным ионом тетрабромфенолсульфофталеина и ионом гидроксила это отношение равно 2 9 и 3 6 для водно-этанольной и водно-метанольной смесей соответственно. Для реакции же между ионом аммония и цианат-ионом это отношение оказывается равным 7 0 и 10 9 для водных смесей с метанолом и с этиленгликолем соответственно. [24]
При оттитровывании персульфат-ионов солью железа к анализируемому раствору прибавляют в избытке титрованный раствор соли железа ( П) и соль серебра, каталитически ускоряющую реакцию восстановления персульфата. Определению мешают органические вещества, так как реакция между персульфат-ионами и Fe ( II) индуцирует окисление органических веществ. Бромиды подавляют такие индуцированные реакции окиеления. Разработан [1003] метод определения персульфат-ионов в присутствии этанола, метанола, аллилацетата, аллилового спирта и метил-изопропиенилкетона с применением бромида натрия в качестве ингибитора индуцированных реакций. [25]
В табл. 2 представлены электрохимические свойства некоторых окислителей, применяемых или имеющих перспективу применения в ХИТ. Высокие положительные значения потенциалов имеют многие окислители: фтор, персульфат-ион, перекись водорода, двуокись свинца, бромноватая, хромовая и хлорная кислоты и пр. Однако равновесные потенциалы, значительно положительнее потенциала кислородного электрода, в водных растворах электролитов не могут установиться из-за протекания реакций с водой. В результате возникает смешанный потенциал. [26]
Если испытание на гидроксиламин проводят в его смесях с большим избытком гидразина, то большую часть последнего можно предварительно осадить при помощи салицилальдегида. Гидроксиламин конденсируется с формальдегидом, и продукт конденсации под действием перекиси водорода или персульфат-иона переходит в формгидроксамовую кислоту. В цветных реакциях гидразина и гидроксиламина с динитробензолами проявляются их восстановительные свойства. В отсутствие гидразина для определения гидроксиламина можно использовать салицилальдегид и ион двухвалентной меди; при этом образуется внутрикомплексное соединение меди с салицил-альдоксимом. При добавлении гидроксиламина к щелочному раствору 8-оксихинолина получается 5-амино - 8-оксихинолин, окисляющийся в присутствии воздуха и конденсирующийся с другой молекулой 8-оксихинолина с образованием кислотно-основного индикатора индоксина. [27]
 |
Хронопотенциограммы восстановления персульфат-ионов на платиновом проволочном электроде. [28] |
При этом обращает на себя внимание аномальная форма ф - / - кривых. Авторы [233] подробно исследовали влияние различных условий на Ф - / - кривые восстановления персульфат-иона: состояния поверхности электрода, рН раствора, концентрации фонового электролита, материала электрода. Катодная активация поверхности электрода приводит к появлению ф - / - кривых ( рис. 5 - 12а, кривые 2 и 3) с периодическими осцилляциями. [29]
Чаще, однако, марганец окисляют до Mn ( VII) с предшествующим осаждением ( если это необходимо) из слабощелочных растворов в виде МпС ШО) с применением в качестве коллектора железа или магния. Перманганат получают окислением соединений марганца периодат-ионом в горячей азотной или серной кислоте или же персульфат-ионом в кипящей смеси фосфорной и азотной кислот, содержащей следы серебра. Перманганат можно затем определить непосредственно спектрофото-метрированием или, с большей чувствительностью, косвенно по окислению веществ типа бензидина, лейкооснования малахитового зеленого, о-толидина или 4 4 -тетраметилдиаминотрифенил-метана; при этом образуются окрашенные продукты. [30]
Страницы: 1 2 3 4