Плотность - неспаренный электрон
Cтраница 4
Неспаренный электрон находится на ороиталк у, поэтому можно предсказать, что плотность неспаренного электрона на концевом атоме углерода С1 равна рг. С - не должно быть плотности неспаренного электрона, и в отсутствие какого-либо вида спиновой поляризации. [46]
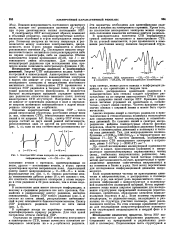 |
Спектры ЭПР атома водорода ( о и макрорадикала полиформальдегида - О-СН-О - ( б.| Спектры ЭПР срединного - СН8 - СН-СН2 - ( о и концевого - CHSCHS ( б макрорадикалов полиэтилена. [47] |
Определив по спектрам ЭПР константы изотропного и анизотропного СТВ, можно вычислить плотности неспаренного электрона на s - и р-орбиталях радикала. [48]
Уменьшение ра при наличии ОН-группы связано, по-видимому, с появлением некоторой плотности неспаренного электрона на атоме кислорода. [49]
Чтобы разрешить этот парадокс, придется пересмотреть изложенные ранее представления о природе плотности неспаренного электрона. Предполагалось, что когда электрон добавляется к молекуле с образованием отрицательного иона, это никак не влияет на другие электроны в молекуле. В этом случае плотность электронного спина ( или спиновая плотность) в точности равна плотности добавленного неспаренного электрона. На самом же деле введение электрона извне слабо влияет на все другие электроны в молекуле. Таким образом, спиновая плотность не совпадает с плотностью неспаренного электрона. Вот почему мы осторожно использовали именно последний термин, пока рассмотрение проводилось в рамках теории МОХ. [50]
 |
Спектры ЭПР хлорзамещенных семихино-нов. [51] |
С с двумя электронами с-связи С - Н на протоне может возникнуть некоторая плотность неспаренного электрона в s - состоянии. [52]
Нечетные альтернантные углеводородные радикалы обладают тем удобным свойством, что можно легко рассчитать плотность неспаренного электрона без определения коэффициентов в молекулярных орбитальных функциях. На примере аллильного радикала II ( простейшего радикала такого типа) видно, что для несвязывающих молекулярных орбиталей i 2 ( рис. 5 - 2) коэффициенты в атомных функциях для непомеченных звездочкой положений равны нулю; сумма коэффициентов для соседних положений также равна нулю. [53]
В первом приближении такая конфигурация не может привести к появлению отличной от нуля плотности неспаренного электрона и, следовательно, изотропного СТВ с а-протонами. [54]
Спиновая и электронная плотности в общем случае являются функциями многих электронов, тогда как плотность неспаренного электрона по своему определению является одноэлектронной функцией. Следовательно, для одного неспаренного электрона, если не учитывать электронного взаимодействия в радикале, функция плотности неспаренного электрона совпадает с функцией спиновой плотности. При этом в любой точке пространства плотность неспаренного электрона положительна. [55]
Таким образом, приведенные выше факты показывают, что благодаря взаимосвязи зарядовой и спиновой плотностей неспаренного электрона последняя может служить критерием реакционной способности феноксильных радикалов. Это позволяет предвидеть возможные направления радикальных реакций, предсказывать строение и соотношение конечных продуктов. Естественно, что при этом необходимо учитывать полярные и стерические эффекты заместителей, которые часто вызывают аномальное, на первый взгляд, течение реакций. Большую информацию могут дать результаты, полученные при использовании корреляционных уравнений, отражающих влияние полярных факторов на реакционную способность мо-лекул и радикалов. Так, при исследовании реакции а ос-дифенил-пикрилгидразила с различными фенолами было показано 15в - 157, что с увеличением электроноакцепторности заместителей в феноле константа скорости гомолитического отрыва атома водорода от гидроксильной группы фенола уменьшается. [56]
Селективность процесса димеризации кетильных радикалов и анион-радикалов определяется электронной структурой частиц ( характером делокализации плотности неспаренного электрона) и стерическими факторами, а также зависит от состава раствора и его температуры. [57]
В связи с этим величина А в многоатомных системах позволяет в принципе нарисовать распределение плотности неспаренного электрона у ядра. [58]
Однако расстояние между компонентами дублета равно 16 з; это связано с тем, что плотность неспаренного электрона у атома водорода в этом радикале в 32 раза меньше, чем в атоме водорода. [59]
Однако расстояние между компонентами дублета равно 16 э; это связано с тем, что плотность неспаренного электрона у атома водорода в этом радикале в 32 раза меньше, чем в атоме водорода. [60]
Страницы: 1 2 3 4 5