Л-электронная плотность
Cтраница 2
Определив с помощью метода МО распределение л-электронной плотности и зная геометрию молекулы, можно вычислить диполь-ный момент, обусловленный распределением л-электронов. [16]
В 9Я - изомере ( 50) л-электронная плотность смещена из центрального ядра, в котором имеется 7 л-злектронов, в крайнее имидазольное и в меньшей степени в бензольное ядра. В 1Я - изомере ( 51) смещение электронов идет в обратном направлении, в результате чего некоторые реакции электрофиль-ного замещения протекают даже по бензольному кольцу. [17]
Поскольку величина сверхтонкого расщепления используется для определения л-электронной плотности [52], сильное влияние растворителя может обесценить эти расчеты. Френкель показал, что имеющиеся данные по влиянию растворителя можно объяснить с помощью простой модели и в качестве первого приближения выдвинул предположение о том, что изменения в величинах расщепления возникают исключительно вследствие перераспределения я-электронной плотности. Была сделана попытка получить ответ на поставленный вопрос с помощью теории МО. Влияние растворителя на сверхтонкое расщепление в семихиноне было объяснено в предположении, что растворитель изменяет электроотрицательность атомов кислорода. [18]
Другим важным типом взаимного влияния атомов является смещение л-электронной плотности к более электроотрицательному атому или группе атомов. Если в цепи связанных атомов, кроме ст-электронов, имеются только я-электроны, то введение в сопряженную я-систему таких атомов более электронодонорного или же электроноакцепторного атома вызовет поляризацию Tt-системы. [19]
 |
Расположение в пространстве ядер атомов углерода в молекуле метилциклопропена. [20] |
Таким образом, определив при помощи метода МОХ распределение л-электронной плотности и зная геометрию молекулы, можно вычислить дипольный момент, обусловленный распределением я-элек-тронов. [21]
Как видно, электронодонорные алкильные группы, вызывающие повышение л-электронной плотности в алкене, значительно увеличивают скоость еакции. [22]
Введение заместителя в положение 6 триазинового кольца незначительно увеличивает л-электронную плотность на втором атоме азота кольца. [23]
 |
Физические константы некоторых галогеиуглеводородов. [24] |
Неподеленная электронная пара вступает в сопряжение и это вызывает смещение л-электронной плотности от атома галогена в сторону углеродных атомов. [25]
Как и в случае индуктивного эффекта, группы, смещающие л-электронную плотность в сторону системы, проявляют С-эффект. Наоборот, группы, вызывающие такое смещение в свою сторону, обладают - С-эффектом. Сопряжение связей в нереагирующей молекуле называется статическим эффектом сопряжения. При взаимодействии молекулы, имеющей систему сопряженных связей, с атакующим реагентом в этой системе происходят глубокие изменения, связанные с перераспределением электронной плотности. В этом случае проявляется динамический эффект сопряжения ( см. с. Примером влияния эффекта сопряжения на направление реакции может служить реакция ненасыщенного альдегида ( акролеина) с бромистым водородом. [26]
Таким образом, чем агрессивнее электрофильный агент и чем больше сосредоточена л-электронная плотность в ароматическом кольце субстрата, тем легче образуется и тем более устойчив поручающийся о-комплекс. [27]
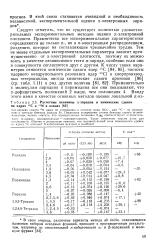 |
Расчетные величины я-зарядов и химические сдвиги на ядрах 13С и 15N в азинах. [28] |
Следует отметить, что не существует полностью удовлетворительных экспериментальных методов оценки л-электронной плотности. Практически все экспериментальные характеристики определяются не только я -, но и ог-электронным распределением, разделить которые на составляющие чрезвычайно трудно. Тем не менее отдельные экспериментальные параметры зависят преимущественно от я-электронной плотности, поэтому их можно взять в качестве независимого теста я-заряда, особенно если они в совокупности согласуются друг с другом. К числу таких параметров относятся химические сдвиги ядер 13С [84, 85], частоты ядерного квадрупольного резонанса ядер 35С1 в хлорпроизвод-ных гетероциклов, иногда химические сдвиги протонов [86] ( ср. [29]
В тетрафторэтене электроотрицательные атомы фтора на столько сильно оттягивают на себя л-электронную плотность, что это соединение способно взаимодействовать даже с таким слабым нуклеофилом, как спирт, и, напротив, неспособно присоединять бромоаодород. [30]
Страницы: 1 2 3 4