Поведение - растворенное вещество
Cтраница 2
Таким образом, для интерпретации поведения растворенных веществ в различных растворителях следует оценивать донорные свойства растворителя лишь после проверки всех имеющихся количественных данных. Наибольшее значение следует придавать результатам, которые получены с кислотами, по своим свойствам более всего похожими на рассматриваемое растворенное вещество. [16]
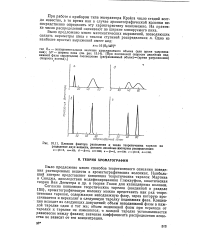 |
Влияние фактора разделения и числа теоретических тарелок на разделение двух веществ, дающих линейные изотермы распределения. [17] |
Было предложено много способов теоретического описания поведения растворенных веществ в хроматографических колонках. Наибольший интерес представляет концепция теоретических тарелок Мартина и Синджа, впоследствии модифицированная Глюкауфом, кинетическая теория Ван Деемтера и др. и теория Голэя для капиллярных колонок. [18]
Приведенные выше уравнения пригодны для характеристики поведения жидких растворенных веществ, однако для твердых растворенных веществ, особенно для электролитов, более удобна иная форма этих уравнений. [19]
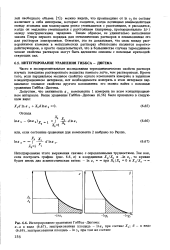 |
Интегрирование уравнения Гиббса-Дюгема. [20] |
Часто в экспериментальном исследовании термодинамических свойств раствора изучать поведение растворенного вещества намного легче, чем растворителя. Кроме того, если парциальное мольное свойство одного компонента измерено в заданном концентрационном интервале, нет необходимости измерять в этом интервале парциальное мольное свойство другого компонента: его можно найти с помощью уравнения Гиббса-Дюгема. [21]
Коэффициент активности - ys является мерой уклонения в поведении растворенного вещества от того его состояния, которое оно имеет в бесконечно разбавленном растворе, когда отсутствуют силы взаимодействия между его молекулами. [22]
Несмотря на то, что трудно ожидать большого различия в поведении растворенного вещества в воде и оксиде дейтерия, тем не менее заметное различие наблюдается. Измерены константы ионизации [52] ряда органических и неорганических кислот в D2O; они оказались меньше, чем в воде, разница находится в пределах 1 единицы р / С. [23]
Он прозорливо отмечал, что недостаточно только физического подхода для объяснения поведения растворенного вещества. Согласно Менделееву, растворение вещества сопровождается проявлением химического сродства между растворенным веществом и растворителем и вызывает образование сольватов различного состава. Многочисленные исследования водных и неводных растворов подтвердили обоснованность взглядов Менделеева. [24]
Как было указано выше, одним из главных факторов, влияющих на поведение растворенного вещества в растворе ( например, СН3СООН), способного проявлять различную степень диссоциации в разных растворителях, и даже диссоциировать по разному типу ( как кислота, основание), является химическая природа растворителя, а не только его диэлектрическая проницаемость. [25]
 |
Схема диссоциации окислов в растворе. [26] |
В реальном случае взаимодействие между молекулами растворителя и растворенного вещества влияет на поведение растворенного вещества в растворе. [27]
Особое место среди дифференцирующих растворителей занимают диполярные апротонные растворители, оказывающие весьма существенное влияние на поведение растворенного вещества при образовании раствора, обусловленное специфическим взаимодействием ( межмолекулярным, ион-дипольным, донорно-акцепторным), структурой и природой смешиваемых веществ. Например, сильные кислоты ( за исключением хлорной) в ДАР становятся слабыми, диссоциация оснований сильно уменьшается. [28]
 |
Термодинамические данные для характеристики различных областей существования ге. п - азоксианизола ( кДж / моль [ 27J. [29] |
Таким образом, газохроматографические величины удерживания непосредственно связаны с предельным коэффициентом активности - ключевым параметром термодинамики, определяющим отклонение поведения растворенного вещества от описываемого законом Рауля. Однако приведенные уравнения отражают эту связь в упрощенной форме. [30]
Страницы: 1 2 3 4