Экстракционное поведение
Cтраница 1
Экстракционное поведение определяется состоянием палладия в водных роданидных растворах. Образующийся красный комплекс способен существовать не только в кислых ( широкий диапазон концентраций НС1) [1227], но и в слабощелочных ( до рН 8) [1231] растворах. Поэтому экстракцию его осуществляют как из кислых ( обычно солянокислых), так и из щелочных [1231] растворов. [1]
Экстракционное поведение некоторых из органических систем ионных ассоциатов ( 26) также можно описать просто. В таких системах растворитель играет физическую роль: он не реагирует с металлом или реагентом. Избыток требуемого органического реагента обычно настолько мал, что при описании равновесий не возникает осложнений благодаря высоким и переменным концентрациям. С другой стороны, ионные неорганические соединения ( 16) при экстракционном равновесии представляют собой очень сложные системы. Кислородсодержащий растворитель взаимодействует с металлом и даже с реагентом. [2]
Экстракционное поведение иридия в этих состояниях окисления сильно различается. [3]
Экстракционное поведение палладия при использовании окиси мезитила, ТБФ, производных пиразолона и в присутствии SnCl2 по характеру аналогично поведению платины ( ГУ) ( стр. [4]
Экстракционное поведение ртути ( П) в этих системах подобно рассмотренному для хлоридных систем. Одновременно со ртутью способны извлекаться многие элементы и достаточно избирательная экстракция, по-видимому, осуществима лишь из нейтральных растворов. [5]
Экстракционное поведение цинка тесно связано с состоянием его в хлоридных водных растворах. Это состояние характеризуется способностью элемента образовывать, по-видимому, четыре малоустойчивых моноядерных комплекса: ZnCl, ZnCla, ZnCls и ZnCl - ( данные об их числе и устойчивости довольно противоречивы) и заметной склонностью образовывать гидроксокомплексы. [6]
Экстракционное поведение урана и плутония в разных валентных состояниях весьма различно, что и используется при отделении их друг от друга, а также от осколочных элементов. [7]
 |
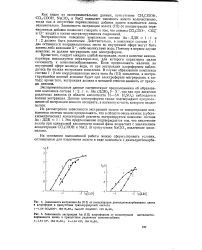
Экстракция W ( VI из хлоридного раствора 0 01 М растворами ДАППМ в дихлорэтане ( /, 2 и хлороформе ( 3, 4. [8] |
Экстракционное поведение золота при извлечении его из хлоридного и иодидного растворов аналогично поведению платины: лучше всего оно извлекается из иодидного раствора. [9]
Экстракционное поведение ассоциатов перренат-иона с тетра-фенилфосфонием [1219] и трифенилбензилфосфонием [1220] аналогично. В качестве растворителя также используется хлороформ. Однако извлечение ассоциатов с тетрафенилфосфонием возможно при более высокой концентрации хлорид-ионов. [10]
Экстракционное поведение комплексов состава Аи: ДДК 1: 1 и 1: 2 должно быть различным. Действительно, в комплексе состава 1: 1 два оставшихся координационных места во внутренней сфере могут быть заняты либо анионами Х -, либо молекулами воды. Поэтому в первом случае комплекс не должен мигрировать при электрофорезе. [12]
Сравнение экстракционного поведения гидрохинона, резорцина и пирокатехина при их экстракции из водных растворов метил-шрет-бутиловым эфиром / / Интеграция науки и высшего образования био - и органическая химия. [13]
Изучение экстракционного поведения ванадия ( III) в условиях, которые рассматривались для ванадия ( IV), показало, что ванадий ( III) количественно элюируется в первых трех свободных объемах растворов всех приведенных комплексующих агентов. Ввиду того, что предполагаемые для анализа образцы представляли собой расплавы хлоридов натрия, калия, рубидия, цезия в различных сочетаниях, содержащие хлориды ванадия, было рассмотрено влияние этих ионов на экстракционную схему разделения ионов, ванадия при использовании сульфосалициловой кислоты в качестве комплексующего агента. [14]
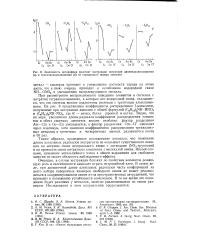 |
Зависимость логарифмов констант экстракции нитратами диоктилалкиламмония ( а и триоктилалкиламмония ( б от порядкового номера элемента. [15] |
Страницы: 1 2 3 4