Экстракционное поведение
Cтраница 2
При рассмотрении экстракционного поведения элементов в системах с нитратом тетраалкиламмония, в которых нет водородной связи, оказывается, что эти системы вполне аналогичны системам с третичным алкиламмо-нием. На рис. 8 представлены коэффициенты распределения / - элементов, полученные при экстракции аминами с общей формулой ( C8H17) 2NR - HNO3 и ( C8H17) 3NR - NO3, где R - метил, бутил ( пропил) и октил. Видно, что по мере увеличения длины радикала коэффициент распределения элементов в обеих системах меняется вполне симбатно: фактор разделения Am-Cm и Се-Eu уменьшается, а фактор разделения Cm-Cf проходит через максимум, хотя значения коэффициентов распределения трехвалентных металлов в третичных и четвертичных аминах различаются почти в 50 раз. [16]
Результаты изучения экстракционного поведения индивидуальных элементов, полученные, например, авторами работы [26], исследовавшими экстракцию большого числа элементов из 5 М НВг диизопропиловым эфиром, нельзя распространять на совместную экстракцию элементов. [17]
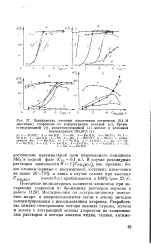 |
Зависимость степени извлечения элементов ( 0 1 М. [18] |
Исследования по экстракционному поведению макро - и микрокомпонентов легли в основу методов концентрирования с использованием хлорекса. [19]
Различие в экстракционном поведении четных и нечетных РЗ, наблюдавшееся Мак-Кеем в кислых растворах [9], не находит еще достаточно ясного объяснения и, по-видимому, связано с тонким различием электронной структуры РЗ. [20]
Несмотря на то что экстракционное поведение большинства кислых экетрагентов в жидкостных экстракционных системах изучено довольно хорошо, любое сколько-нибудь полное описание хрО Матографического процесса на основе данных по экстракции в значительной степени ограничено по двум причинам: во-первых, обычно очень трудно оценить реальное состояние исследуемого элемента в водных растворах и, во-вторых, представления о термодинамических свойствах неподвижных фаз очень ограниченны. [21]
Авторами собраны данные об экстракционном поведении более 40 элементов. Подробно рассмотрено практическое использование экстракции из галогенидных растворов и даны многочисленные примеры разделения и концентрирования элементов. Монография основана на результатах исследований авторов и широком литературном материале, который обобщен и критически оценен. [22]
Концентрация кислот и роданидов определяет экстракционное поведение кадмия. Зависимость D / ( cNH4sci) выражается кривыми с максимумом ( ДАПМ, CNHscN - l 2 M, Сн2зо4 0 5 М [954]), a D / ( сн) восходящими ( ДАПМ) кривыми. [23]
Оценено влияние гидролиза титана на его экстракционное поведение. [24]
Полученные результаты дополняют имеющиеся сведения об экстракционном поведении ионов урана, поскольку использование неразбавленных экстрагентов налагает на исследователя ряд трудностей как при выполнении работы, так и при описании процесса экстракции. Метод колоночной распределительной хроматографии позволяет преодолеть эти трудности и, таким образом, открывает дополнительные возможности для получения новых экспериментальных данных о коэффициентах распределения элементов. Эти результаты в сочетании с имеющимися в литературе сведениями о состоянии исследуемых ионов в растворе могут стать основой для выявления механизма экстракционного процесса. [25]
В работе [372] опубликованы ценные сведения по экстракционному поведению сольватов нитрозилрутения с ТБФ. [26]
Различные валентные состояния металла часто отличаются по стереохимии, экстракционному поведению и другим свойствам их комплексов, а также по типам лигандов, с которыми они образуют наиболее прочные комплексы. В таких случаях в качестве основы высокоизбирательных аналитических методов можно использовать экстракцию ( предпочтительно), ионный обмен, осаждение или некоторые другие приемы с последующим окислением или восстановлением и взаимодействием с соответствующим лигандом. [27]
Если заряд и тип координации экстрагируемых катионов одинаковы, то и экстракционное поведение их сходно: периферийные части объемистых хелатных комплексов одинаковы. [28]
Усложнение состава водной фазы, очевидно, может значительно влиять на экстракционное поведение металлов. Во многих случаях такое влияние объясняют достаточно просто, например, тем, что добавление к раствору, содержащему только электролиты, не способные к образованию комплексов, реагентов, которые, напротив, образуют анионные комплексы, способствует экстракции. Но иногда эффекты не так очевидны или не столь легко объяснимы. [29]
Гипотеза аналогий - простое, но весьма ценное обобщение, позволяющее в ряде случаев предвидеть экстракционное поведение элементов и оценивать возможность их разделения. [30]
Страницы: 1 2 3 4