Кинетическое поведение
Cтраница 3
Для обнаружения и изучения кинетического поведения многоатомных радикалов предложен новый способ применения спектрометра ЭПР. Кинетика газофазной реакции изучается по скорости накопления многоатомных радикалов на охлажденной поверхности. По кинетике образования радикала НО2 и стабильных продуктов изучен детальный механизм окисления формальдегида. Определены константы скорости реакций: НО2 СН2О Н2О2 НСО и НОг СО СО2 ОН. При низкотемпературном окислении пропана вымораживается В. С повышением температуры концентрация КОг-радикалов достигает максимума в зоне отрицательного температурного коэффициента скорости реакции и затем падает. [31]
По фазовому составу и кинетическому поведению комплексные металлоорганические катализаторы авторы работы [111] условно предлагают разделить на три группы. [32]
По фазовому составу и кинетическому поведению комплексные металлоорганические катализаторы условно можно разделить на три группы. К первой группе относятся истинно гетерогенные каталитические системы, один из компонентов которых практически нерастворим в реакционной среде. [33]
Если реакция действительно подчиняется кинетическому поведению типа ( 72), этот график будет иметь вид прямой линии, тангенс угла наклона которой равен KZ, с отрезком, отсекаемым от оси ординат, равным KI. Аналогичные графики могут быть непосредственно построены для других типов кинетической зависимости смешанного порядка. [34]
Межмолекулярное взаимодействие влияет прежде всего на кинетическое поведение макромолекул. Так, наличие межмолекулярных сил определяет стеклование полимеров в блоке. Для высокоэластической деформации необходимо наличие гибкости у полимерных цепей. Поэтому при тех температурах, при которых межмолекулярные силы способны фиксировать положение звеньев макромолекул в блоке, высокоэластическая деформация невозможна и полимер находится в стеклообразном состоянии. Соответствующие представления были развиты / Курковым [37] при построении теории пластификации полимеров. [35]
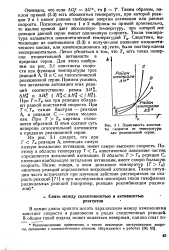 |
Зависимость константы скорости от температуры для реакционной серии. [36] |
Поэтому в области температур Т Тп кинетическое поведение частиц определяется энтальпией активации. В области Т Ги реакция С, имеющая наибольшую энтальпию активации, имеет самую большую скорость. Иначе говоря, в этом диапазоне температур ( Т Ги) кинетика реакций определяется энтропией активации. [37]
Действительно, системы уравнений, описывающих кинетическое поведение реакции для двух обсуждаемых механизмов, различны, следовательно, должны наблюдаться различия и в уравнениях, представляющих решение этих систем. [38]
Еще два замечания Связаны с особенностями кинетического поведения застойной зоны: 1) стационарность в ней устанавливается только спустя длительное время; 2) степень полидишерсности будет зависеть от соотношения потоков и объемов активной и застойной зон. [39]
Еще два замечания связаны с особенностями кинетического поведения мертвого объема: 1) стационарность в нем установится только спустя длительное время; 2) показатель полидисперсности будет зависеть от соотношения потоков и объемов активного и мертвого реакционных пространств. [40]
Явной корреляции между термодинамической устойчивостью и кинетическим поведением комплексов яе существует. В первом ряду переходных металлов октаэдрические комплексы жрома ( Ш) и кобальта ( III) обычно оказываются инертными ( полупериод жизни равен нескольким суткам или даже неделям), а комплексы ионов других металлов являются лабильными ( ср. [41]
Обнаруженное значительное влияние стереохимической конфигурации полимера на его кинетическое поведение Ремп, однако, не обсуждает. [42]
 |
Энергии активации реакций, проводимых гомогенно в газовой фазе и каталитически на металлах. [43] |
Отдельную группу химических процессов составляют цепные реакции, сложное кинетическое поведение которых обуславливает целый ряд необычных явлений. [44]
Многие органические соединения проявляют аналогичное химическое, но различное кинетическое поведение. Это свойство используется при анализе смесей изомеров и других близких по свойствам соединений. [45]
Страницы: 1 2 3 4