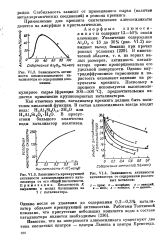
Поверхность - алюмосиликат
Cтраница 1
Поверхность алюмосиликатов еще более кислая, чем поверхность окиси алюминия, но эта кислотность менее чувствительна к отравлению водой. Много дискутировался вопрос о том, чем вызывается кислотность алюмосиликатов: бренстедовскими или льюисовскими кислотными центрами. Этот вопрос окончательно не решен, хотя имеются данные, указывающие, что присутствуют оба типа кислотных центров. Этим объясняется тот факт, что каталитическая активность в различных реакциях может быть селективно отравлена различными реагентами. [1]
 |
Теплота смачивания водой в зависимости от содержания структурной воды для черенковой оииси алюминия. Черные точки - вторично гидратированные образцы. [2] |
Поверхность алюмосиликатов является, по-видимому, более неоднородной, чем поверхность силикагеля. [3]
При дегидратации поверхности алюмосиликатов нагреванием до высокой температуры происходит удаление воды с брен-стедовского кислотного центра. При этом открывается ион алюминия, являющийся льюисовским кислотным центром. Дегидратированная поверхность может проявлять бренстедовскую и льюисовскую кислотность в зависимости от условий предварительной обработки. Максимальная концентрация бренстедовских кислотных центров наблюдается при содержании оксида алюминия 25 % ( мае. [4]
Таким образом, поверхность алюмосиликата имеет структуру, на которой обменные центры являются и активными центрами и их в 3 раза меньше, чем общее число кремневых центров. [5]
Известно, что на поверхности алюмосиликата существуют два типа кислотных центров - центры Льюиса и центры Бренстеда. [7]
Выводы о донорно-акцепторном взаимодействии мономера с поверхностью катионзамещенных алюмосиликатов подтверждаются характерными особенностями адсорбции слабого п-донора ( бензола) на атионзамещенном монтмориллоните. Характер изотерм адсорбции бензола свидетельствует о специфическом адсорбционном взаимодействии его с поверхностью, которое может быть обусловлено образованием поверхностных я-комплексов. Еще более вероятно образование поверхностных донорно-акцепторных связей при адсорбции на та ях катионзамещенных катализаторах стирола. [8]
Аналогичные опыты были проведены по адсорбции пиридина на поверхности алюмосиликата. Поглощение в этой области не является результатом проявления колебаний с участием атомов азота, скорее оно связано с колебаниями, в которых принимают участие атомы углерода цикла. [9]
Ароматические углеводороды в основном неполярны, и адсорбция их на поверхности алюмосиликатов или силикагелей является следствием возникновения дипольного момента под влиянием электростатического поля поверхности адсорбента. В этом случае основные закономерности, отмеченные выше в главе о растворимости углеводородов, касающиеся влияния строения ароматических углеводородов на индуцирование в них дипольного момента под влиянием электростатического поля полярного растворителя, при-ложимы и к разбираемому вопросу. [10]
Спектроскопически Уэбб [88] показал, что при адсорбции дифенил-этилена на поверхности алюмосиликата образуются ионы карбония ( катионы дифенилэтила) и комплексы с переносом заряда. [11]
Интересно, что количество оставшейся воды, которая удерживается на единице поверхности алюмосиликата, почти такое же, какое удерживает окись кремния в области температур от 400 до 500 С. [12]
На примере металлоорганических соединений хрома, при химическом связывании которых с поверхностью алюмосиликата или силикагеля протекает полимеризация, изучен механизм образования r awc - полимеров и сополимеров диенов. Металлоорганический катализ на поверхности открывает новые перспективы и для полимеризации олефинов. [13]
Радиохимическим методом, методом блокировки аммиаком и при помощи дейтериепой метки была исследована поверхность алюмосиликата, окиси алюминия и окиси магния с целью изучения природы центров, ответственных за изомеризацию и полимеризацию бутепа-1. Изучение поведения бутена-1 на алюмосиликате показало, что происходит быстрое образование адсорбированного полимерного комплекса, которое заканчивается в течение нескольких минут. Результаты опытов по блокировке аммиаком показали, что данный полимерный комплекс является активным участком поверхности для протекания реакции изомеризации. При давлении 50 мм рт. ст. наиболее высоком из исследованных, бутен адсорбируется в среднем в виде пентамера. Результаты ориентировочных исследований, проведенных с окисью алюминия и окисью магния, показали, что механизм изомеризации на этих катализаторах существенно отличается от механизма изомеризации на алюмосиликате. [14]
Кривая 3, соответствующая поглощению индикатора в адсорбированном состоянии, ясно свидетельствует о кислотном характере поверхности алюмосиликата. Используя различные основные индикаторы - ( табл. 5), Дзисько и др. [12] определили этим методом силу кислотных центров различных смешанных окислов. [15]
Страницы: 1 2 3 4